Conoce a tu sistema inmune (Parte 2): Los mastocitos,Tus guardianes internos: ¿Héroe o enemigo?

La clave está en la ciencia, el cambio en ti.
¿Alguna vez te ha picado un mosquito o una abeja y la piel se te ha inflamado casi al instante? ¿O has empezado a estornudar sin parar apenas entras en una habitación con polvo?
Detrás de estas reacciones está un protagonista diminuto pero explosivo: el mastocito. Imagínalos como soldados repartidos por todo tu cuerpo (en la piel, los pulmones, el intestino) armados con pequeñas mochilas llenas de sustancias químicas. Su trabajo es protegernos, pero a veces, estos soldados se vuelven demasiado sensibles y empiezan a disparar sus alarmas de forma indiscriminada y en todas direcciones (1,2).
Cuando esto ocurre de forma descontrolada, favorece la aparición de inflamación crónica, alergias, del Síndrome de Activación Mastocitaria (MCAS), enfermedades autoinmunes. Vamos a descubrir cómo funcionan y, sobre todo, cómo calmarlos (3,4)
1. ¿Qué es exactamente un mastocito?
El mastocito es una célula de tu sistema inmune que nace en la médula ósea (el tejido blando y esponjoso que se encuentra en el interior de los huesos) y se instala en las "fronteras" de tu cuerpo: la piel y las mucosas (5).
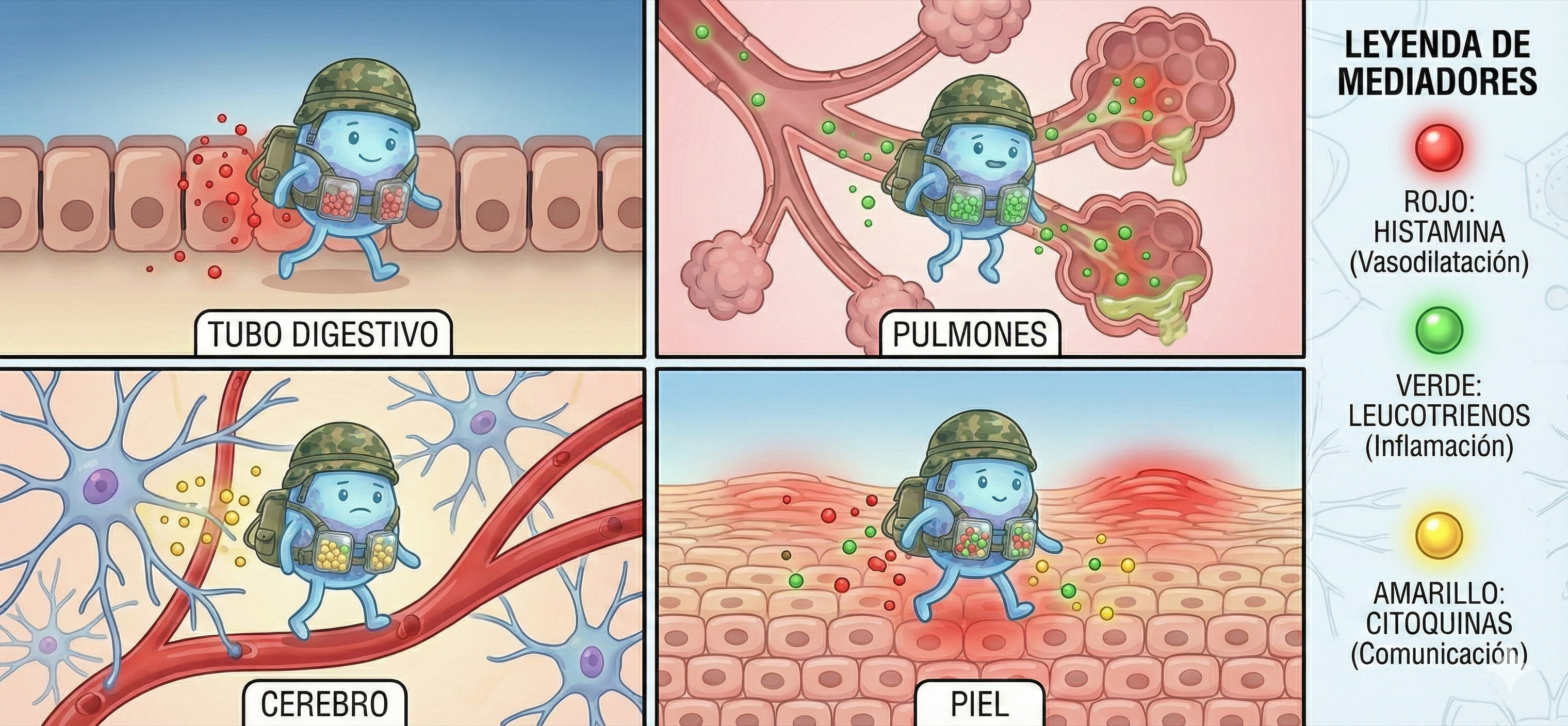
Visualmente, imagina a este soldado portando un chaleco táctico cargado de granadas. Cada una de esas granadas son los gránulos: pequeñas cápsulas de almacenamiento listas para ser liberadas. La granada en sí es el mediador. Al detonar, libera su efecto en el entorno. Algunas granadas contienen histamina (provoca picor, enrojecimiento y moco), otras heparina (modifica la coagulación y la permeabilidad vascular) y otras citoquinas, que actúan como señales de radio llamando a más soldados inmunes al lugar del conflicto (6,2).

Sus funciones: el equilibrio vital
No son los villanos de la historia. En equilibrio, son maestros de la regulación (7,2,1) :
-
Reparación de tejidos: Son esenciales para la cicatrización y la reconstrucción de la piel y mucosas tras una lesión o herida.
-
Acción antiinflamatoria: No solo "encienden las alarmas"; también pueden liberar sustancias (como la IL-10) que ayudan a frenar la inflamación cuando ya no es necesaria, evitando que el cuerpo se ataque a sí mismo. Velo como una señal de “alto al fuego, la guerra ha terminado”.
-
Formación de vasos sanguíneos: Ayudan a crear nuevas rutas de irrigación (angiogénesis) donde el cuerpo necesita nutrientes. Los soldados crean nuevas carreteras por donde poder transitar ante una emergencia.
-
Defensa activa: Nos protegen de forma inteligente contra parásitos, virus y bacterias.
-
Botiquín de emergencia: Actúan como coordinadores que deciden cuándo iniciar una defensa y, lo más importante, cuándo terminarla.
2. ¿Por qué se desequilibran? (Las Causas)
A veces, el "gatillo" de estos soldados se vuelve muy sensible. Esto puede pasar por varias razones:
-
Genética (El manual viene con errores): En condiciones como la mastocitosis, el cuerpo fabrica demasiados mastocitos debido a un error en el gen KIT. Es como si tuvieras un ejército diez veces más grande de lo normal, lo que causa síntomas graves por el simple exceso de células (8).
-
El Estrés (El eje mente-cuerpo): El estrés no está "solo en tu cabeza". El sistema nervioso libera hormonas que le dicen directamente al mastocito: "¡Dispara!". Por eso el asma o la dermatitis empeoran cuando estamos bajo mucha presión (9).
-
Fármacos: Algunos medicamentos (como ciertos antibióticos o analgésicos, AINES en algunos casos) pueden activar al mastocito directamente, sin que seas "alérgico" de forma clásica. Simplemente tocan un botón en su superficie (llamado receptor MRGPRX2) y este libera su carga (10).
-
Acumulación de tejido adiposo (grasa corporal):Se ha observado que el exceso de grasa (especialmente la abdominal) provoca una mayor presencia de mastocitos activos. Estos liberan sustancias que favorecen la resistencia a la insulina y aumentan el riesgo cardíaco, convirtiendo a la grasa en una fuente de inflamación constante (11).
-
El Entorno Moderno: La contaminación del aire (partículas PM2.5)(60), el moho en casa, micotoxinas (12,13) y las infecciones persistentes o prolongadas (como long covid)(14) mantienen a los mastocitos en un estado de alerta roja constante.
-
Otros: vacunas, alcohol, calor y cambios de temperatura (15).
3. Consecuencias: Cuando el guardián nos ataca a nosotros
Un mastocito descontrolado no solo causa estornudos o picazón; puede afectar a casi todo el cuerpo:
-
Alergias Agudas: Ocurren cuando el sistema inmune identifica por error una sustancia inofensiva como una amenaza. Tus mastocitos se "sensibilizan" con anticuerpos IgE y, ante el mínimo contacto, liberan su contenido químico. Esto puede derivar en una anafilaxia, una emergencia donde baja la presión, se cierra la garganta y se requiere atención médica inmediata(16,17,4).
-
Alergias crónicas: : Cuando los mastocitos están constantemente "encendidos", mantienen una inflamación persistente que da lugar a condiciones como el asma, la rinitis, la conjuntivitis o la dermatitis atópica. En estos casos, las células no se apagan, provocando que los pulmones se cierren, la nariz gotee o la piel pique de forma crónica día tras día (18).
-
MCAS (Síndrome de Activación Mastocitaria): Los mastocitos son "hiperactivos" sin un culpable claro. El diagnóstico es complejo porque los síntomas (mareos, taquicardia, diarrea) aparecen y desaparecen, confundiéndose a menudo con ansiedad, depresión o hasta otros diagnósticos como fibromialgia (que puede coexistir) (19,15).
-
Un estudio masivo de 413 pacientes (20) reveló los siguientes datos: que esta condición afecta mayoritariamente a mujeres (69%) y personas de origen caucásico (75%).
-
Los datos llaman mucho la atención: aunque los síntomas suelen aparecer a una edad temprana (mediana de 9 años), el diagnóstico promedio no llega hasta los 49 años.
-
Este retraso de 40 años se debe, en parte, a que los criterios diagnósticos precisos son muy recientes. Pero también responde a la enorme complejidad del cuadro: los pacientes sufren una mediana de 20 síntomas distintos y conviven con unas 11 enfermedades asociadas (comorbilidades). Esta diversidad hace que sus crisis se confundan con múltiples patologías antes de dar con la clave (20)
-
Nota del caso clínico real: En el estudio de Cardona et al., una paciente de 73 años sufrió anafilaxias graves que inicialmente parecían una alergia común a la yuca, pero su triptasa elevada reveló que sus mastocitos ya estaban pre-activados por un problema clonal (SAMM) (21).
-
Inflamación crónica de bajo grado: Esta inflamación es sutil pero constante, dañando arterias y órganos a largo plazo (3,11).
-
Impacto Neurológico y "Cerebro Nublado": La liberación de mediadores en el sistema nervioso central y autónomo contribuye a la fatiga crónica, problemas de memoria y se ha vinculado con cuadros de depresión y ansiedad. Alteración del sistema nervioso autónomo (22).
-
Estado hormonas sexuales: Los mastocitos responden a los cambios en las hormonas sexuales (especialmente los estrógenos). El estradiol puede activarlos rápidamente y aumentar la inflamación, siendo parte de la causa de algunos síntomas premenstruales o alergias/asmas perimenstruales, síntomas exacerbados en endometriosis, otros.(48,49)De hecho, estudios recientes confirman que en la endometriosis el estrógeno actúa como un 'interruptor' directo que obliga al mastocito a liberar sustancias que perpetúan el dolor y la inflamación (51) Esto depende del nivel hormonal y del tejido, no sólo del “ciclo menstrual.Por otra parte, un hallazgo clave de 2023 revela el porqué del dolor: el estrógeno estimula al mastocito a liberar una molécula llamada FGF2 (Factor de Crecimiento de Fibroblastos 2). Esta molécula provoca que los nervios se ramifiquen y se vuelvan hipersensibles, confirmando que el dolor pélvico es una alteración física real impulsada por tus hormonas, no solo una sensación(52).
-
Respuesta exagerada a infecciones: Un mastocito hiperactivo puede causar una respuesta inflamatoria desproporcionada ante virus comunes (como la gripe), haciendo que los síntomas sean mucho más severos de lo normal (14,23,2).
-
Eje Intestino-Cerebro: Los mastocitos actúan como "sensores" que traducen el estrés psicológico en inflamación física y viceversa. La fatiga crónica y el "cerebro nublado" son el resultado de esta comunicación alterada (50).
-
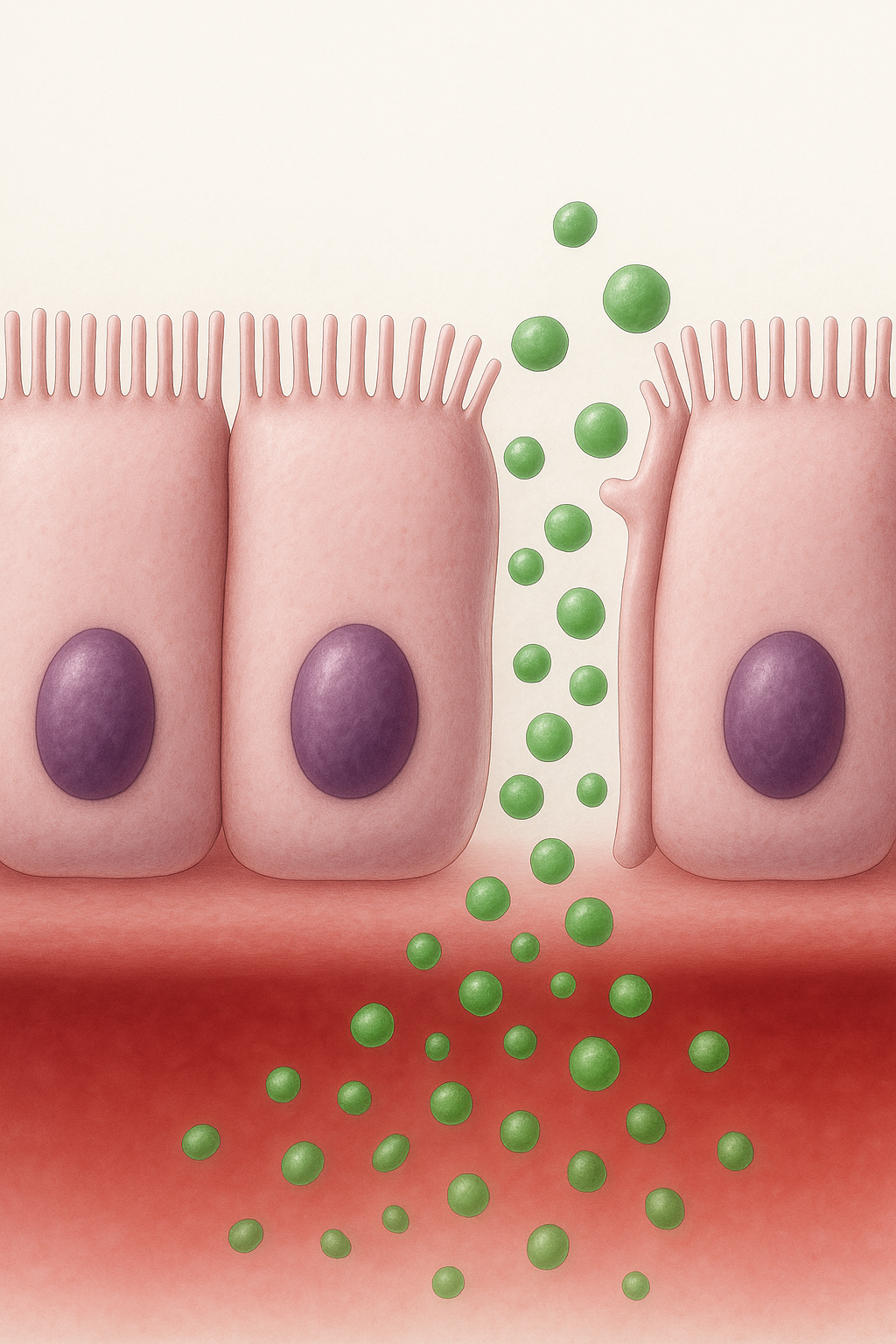
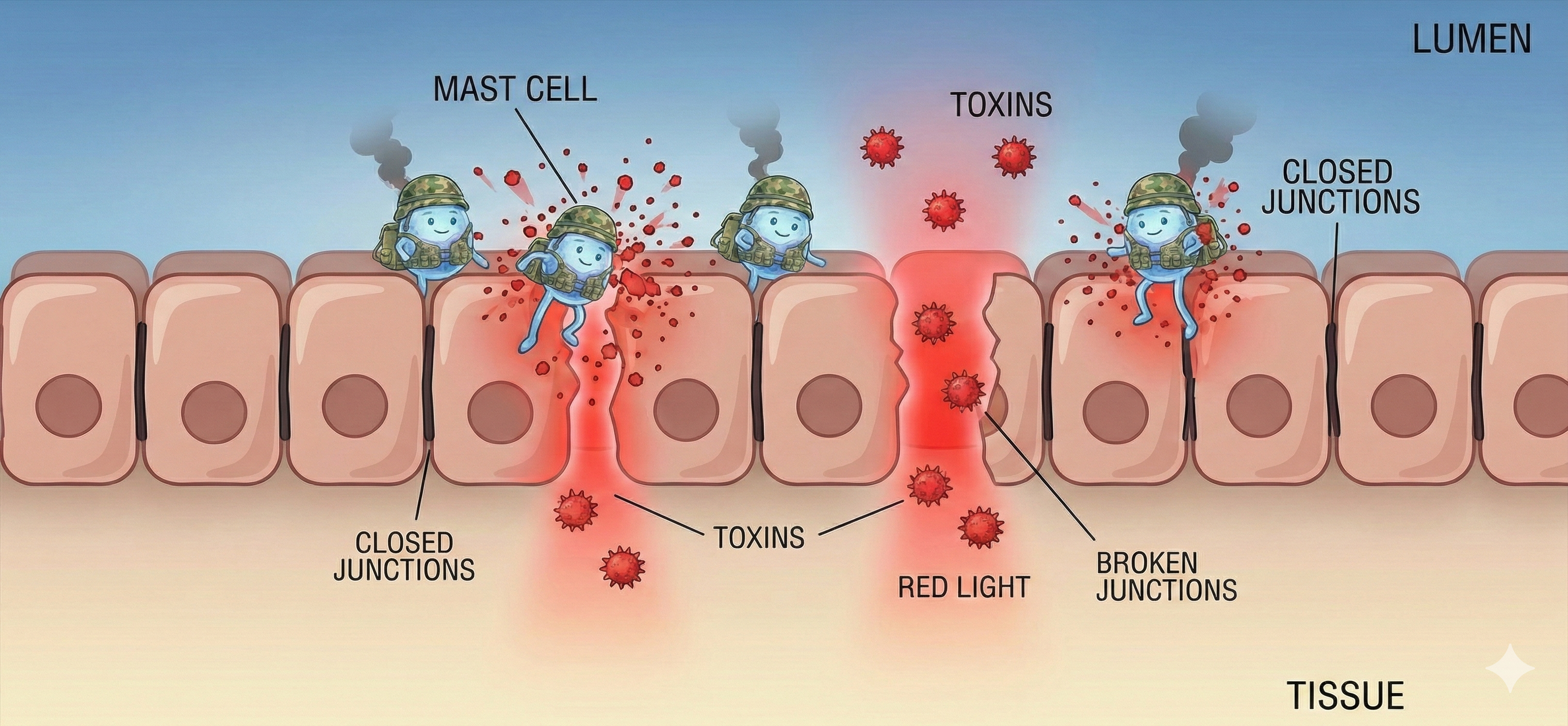
Permeabilidad intestinal: Los mastocitos cuentan con las "puertas" del intestino. Si están fuera de control, estas puertas se abren (intestino permeable), permitiendo que toxinas y otros elementos pasen a la sangre y disparen más inflamación sistémica (24). De hecho, el estrés es un detonante clave: obliga al mastocito a liberar sustancias que disuelven la 'ocludina', el pegamento que debería mantener esas puertas selladas (53).
-
Síntomas digestivos:La presencia de mastocitos irritados en el sistema digestivo puede provocar dolor abdominal tipo cólico, hinchazón, náuseas y cambios drásticos en el ritmo evacuatorio (diarrea o estreñimiento). Al liberar mediadores, estas células alteran la movilidad del intestino y la sensibilidad al dolor, lo que a menudo se confunde con un simple Síndrome de Intestino Irritable (25,26,27).
-
Otros cuadros: Se han visto implicados en problemas de hígado (colangitis)(28) y hasta en la estabilidad de placas en las arterias, aterosclerosis (2).

Analítica y cómo se diagnostica / monitorea
Si sospechas de un problema con tus mastocitos, estos son los parámetros clave que tu médico suele revisar: (29,30).
-
Triptasa sérica: Es la prueba principal. Lo ideal es comparar tu nivel "basal" (en reposo) con el nivel durante una crisis (medido entre 30 minutos y 4 horas después del inicio de los síntomas). Un aumento significativo confirma que los mastocitos se han activado, aunque se considera la prueba estándar, estudios recientes muestran que es poco fiable en el MCAS, ya que solo el 16% de los pacientes presenta niveles elevados. Si sale normal, no se debe descartar el diagnóstico de inmediato(20).
-
Estudios Genéticos: En casos de sospecha de mastocitosis, se busca la mutación del gen KIT (D816V) en sangre o médula ósea, o se analizan pequeñas muestras de tejido para ver si hay acumulaciones anormales de estas células(19). En otros casos genéticos está la Alfa-Triptasemia Hereditaria (HαT), presente en un 6% de la población aproximadamente. Si bien no suele dar problemas/síntomas puede predisponer a reacciones más severas si coexisten otras condiciones(31).
-
Evidencia de activación: Elevación de mediadores durante las crisis (Regla del triptasa basal + 20% + 2)(54) . Sin embargo, dada la baja sensibilidad de la triptasa en el MCAS (20), la medición de heparina y PGD2 cobra un valor fundamental para no dejar pacientes sin diagnóstico.
4. ¿Cómo recuperar el equilibrio? (Medidas de Acción)
A. Alimentación
-
Dieta baja en histamina: Evita temporalmente embutidos, quesos curados, fermentados, mariscos, tomates, espinacas, chocolate, cítricos y alcohol (especialmente vino tinto y cerveza) en periodos de crisis. También es clave evitar las sobras de comida de días anteriores, ya que la histamina aumenta con el tiempo de almacenamiento (por la actividad de bacterias). Como tal la dieta no calma las mastocitos, pero evita sobrecargar a tu sistema con más histamina de la que puede ser capaz de manejar. Puedes ver más en mi post de histamina. La idea de esta dieta más la baja en fodmaps, mencionada justo abajo, es identificar desencadenantes de síntomas (32).
-
Dieta baja en FODMAP: Consiste en reducir temporalmente ciertos carbohidratos fermentables que suelen causar gases y distensión. Al evitar la hinchazón abdominal, se reduce la carga de trabajo del intestino al no tener alimentos que generen irritación o exceso de fermentación que pueda generar daños (27).
-
Flavonoides y antioxidantes: Diversos compuestos naturales presentes en alimentos como la quercetina (manzanas, cebollas),la luteolina, piperina, ayudan a estabilizar a la célula para que no libere sus químicos tan fácilmente sumado a su poder antioxidante y anti inflamatorio. Yo te sugiero que partas con el suplemento antes que el alimento dado que varios de los alimentos que la contienen podrían no ser bien tolerados en periodos de crisis (10,55).

B. Suplementación sugerida:
-
Vitamina D: Más que una vitamina es una hormona. La vitamina D es un potente inmunomodulador que actúa como un "ancla" para los mastocitos. Ayuda a mantener su membrana celular estable y promueve la liberación de señales anti inflamatorias, evitando que las células reaccionen de forma exagerada ante estímulos inofensivos (33,57).
-
Omega-3 (EPA y DHA): Estos ácidos grasos actúan como un "apagafuegos" natural al integrarse directamente en las membranas (la superficie) de las células. Al hacerlo, permiten que se reduzcan la producción de mensajeros químicos inflamatorios, ayudando a tratar el problema desde la raíz (34,56).
-
Zinc: Es un mineral esencial para el crecimiento y la función de las células inmunes. El zinc ayuda a estabilizar la estructura física de los mastocitos; se ha documentado que su deficiencia facilita la ruptura de sus gránulos y la liberación de histamina, por lo que mantener niveles adecuados actúa como un refuerzo preventivo contra la activación espontánea. El zinc también ayuda a reparar las capas del intestino, reduciendo la permeabilidad intestinal (35,36,37,38,39,40).
-
Probióticos: Actúan restaurando la barrera intestinal para evitar que toxinas y bacterias disparen la alerta de los mastocitos digestivos. Cepas específicas, como el Lactobacillus plantarum, han demostrado capacidad para reducir la liberación de histamina y triptasa, calmando la inflamación sistémica desde su origen en el intestino (en ratones por ahora)(41). En un estudio in vitro (uso de células humanas en laboratorio), la cepa lactobacillus rhamnosus LGG y Lc705 ha mostrado reducir la formación de IgE y receptores H4 (receptores de histamina, reciben histamina)(58,59). Estos estudios que encontré son en modelos animales pero no dejan de ser interesantes por su metodología y resultados prometedores.
-
Cromoglicato de sodio: No es un suplemento, sino un fármaco estabilizador del mastocito. Actúa sellando su membrana e impidiendo la liberación de histamina y otros mediadores (básicamente es un candado que impide que el militar pueda sacar de su chaqueta las granadas) por lo que funciona de forma preventiva, antes de que la reacción comience. A diferencia de los antihistamínicos —que actúan después del evento—, requiere uso sostenido y no es tan útil en crisis agudas. Su eficacia es especialmente relevante en síntomas gastrointestinales y, en menor medida, a nivel respiratorio y pulmonar (42,43).
-
Quercetina: En comparación con el cromoglicato de sodio actuaba como un "cemento" externo para reforzar la pared del mastocito (actua fuera de la célula), la quercetina actúa desconectando los cables eléctricos internos (por dentro de la célula) que detonan la explosión de la célula(44), En estudios in vitro ha mostrado ser más eficiente que el cromoglicato, esto en gran parte debido al ser más versátil (aparte de estabilizar mastocitos, tiene poder antioxidante y anti inflamatorio), sin embargo es necesario ver estudios mas potentes (ensayos clínicos) para dar mayor certeza (45).

C. Tratamientos médicos
-
Anticuerpos monoclonales: Considerada terapia de alta precisión. Son fármacos inyectables como el omalizumab que reducen los niveles de IgE circulantes y receptores que activan los mastoctitos en la superficie de estos a los cuales se une la IgE (43,44,45). Reviviendo la analogía del soldado es como si el omalizumab cortará la comunicación (o la reduzca) con el soldado, evitando que lance una señal de ataque. Échale un ojo a la tabla 2 de la referencia (43). Está muy interesante.
-
Inmunoterapia (Vacunas): Consiste en "reeducar" al sistema inmune mediante dosis crecientes de lo que te da alergia (polen, ácaros o veneno de abejas). Con el tiempo, el cuerpo deja de ver estos elementos como enemigos, lo que calma a los mastocitos y reduce drásticamente el riesgo de ataques graves o anafilaxias (15).
D. Estilo de Vida
-
Gestión del Estrés: Técnicas de respiración y cuidado del nervio vago envían señales de seguridad al sistema inmune, calmando la respuesta mastocitaria (9).
-
Ejercicio moderado: El ejercicio extenuante eleva los niveles de histamina y genera procesos inflamatorios de reparación.Esto es un proceso fisiológico normal, pero en casos de activación exagerada de mastocitos, tu cuerpo no tolerará grandes volúmenes de entrenamiento o muy intensos. Evita HIITS largos kilómetros de trote o bici o sesiones de fuerza muy intensas (46,47).
Reflexión Final
Los mastocitos no son tus enemigos; son guardianes que han perdido el rumbo y la tranquilidad. Entender qué los enciende te da el poder de devolverles la ruta y la calma. Recuperar el equilibrio no tiene porque ser una batalla dura, sino un proceso de escucha activa y evidencia científica aplicada.

Referencias
-
Galván-Morales, M. Á., Vizuet-de-Rueda, J. C., Montero-Vargas, J. M., & Teran, L. M. (2025). Role of Mast Cells in Human Health and Disease: Controversies and Novel Therapies. International Journal of Molecular Sciences, 26(18), 8895. https://doi.org/10.3390/ijms26188895
-
Dileepan, K. N., Raveendran, V. V., Sharma, Rishi, Abraham, H., Barua, R., Singh, V., Sharma, Ram, & Sharma, M. (2023). Mast cell-mediated immune regulation in health and disease. Frontiers in Medicine, 10, 1213320. https://doi.org/10.3389/fmed.2023.1213320
-
González-de-Olano, D., & Álvarez-Twose, I. (2018). Mast cells as key players in allergy and inflammation. Journal of Investigational Allergology and Clinical Immunology, 28(6), 365–378. https://doi.org/10.18176/jiaci.0327
-
Thangam, E. B., Jemima, E. A., Singh, H., Baig, M. S., Khan, M., Mathias, C. B., Church, M. K., & Saluja, R. (2018). The role of histamine and histamine receptors in mast cell-mediated allergy and inflammation: The hunt for new therapeutic targets. Frontiers in Immunology, 9, 1873. https://doi.org/10.3389/fimmu.2018.01873
-
Metcalfe, D. D., Baram, D., & Mekori, Y. A. (1997). Mast cells. Physiological Reviews, 77(4), 1033–1079. https://doi.org/10.1152/physrev.1997.77.4.1033
-
Molderings, G. J., & Afrin, L. B. (2023). A survey of the currently known mast cell mediators with potential relevance for therapy of mast cell-induced symptoms. Naunyn-Schmiedeberg's Archives of Pharmacology, 396, 2881–2891. https://doi.org/10.1007/s00210-023-02545-y
-
Wang, X., Zhang, P., Tang, Y., Chen, Y., Zhou, E., & Gao, K. (2024). Mast cells: a double-edged sword in inflammation and fibrosis. Frontiers in Cell and Developmental Biology, 12, 1466491. https://doi.org/10.3389/fcell.2024.1466491
-
Worrall, W. P. M., & Reber, L. L. (2025). Current and future therapeutics targeting mast cells in disease. Pharmacology & Therapeutics, 273, 108892. https://doi.org/10.1016/j.pharmthera.2025.108892
-
Theoharides, T. C. (2020). The impact of psychological stress on mast cells. Annals of Allergy, Asthma & Immunology, 125, 388–392. https://doi.org/10.1016/j.anai.2020.07.007
-
Kumar, M., Duraisamy, K., & Chow, B.-K.-C. (2021). Unlocking the non-IgE-mediated pseudo-allergic reaction puzzle with Mas-related G-protein coupled receptor member X2 (MRGPRX2). Cells, 10(5), 1033. https://doi.org/10.3390/cells10051033
-
Żelechowska, P., Agier, J., Kozłowska, E., & Brzezińska-Błaszczyk, E. (2018). Mast cells participate in chronic low-grade inflammation within adipose tissue. Obesity Reviews: An Official Journal of the International Association for the Study of Obesity, 19(5), 686–697. https://doi.org/10.1111/obr.12670
-
Kritas, S. K., Gallenga, C. E., D Ovidio, C., Ronconi, G., Caraffa, A., Toniato, E., Lauritano, D., & Conti, P. (2018). Impact of mold on mast cell-cytokine immune response. Journal of Biological Regulators and Homeostatic Agents, 32(4), 763–768.
-
Kraft, S., Buchenauer, L., & Polte, T. (2021). Mold, mycotoxins and a dysregulated immune system: A combination of concern? International Journal of Molecular Sciences, 22(22), 12269. https://doi.org/10.3390/ijms222212269
-
Afrin, L. B., Weinstock, L. B., & Molderings, G. J. (2020). Covid-19 hyperinflammation and post-Covid-19 illness may be rooted in mast cell activation syndrome. International Journal of Infectious Diseases: IJID: Official Publication of the International Society for Infectious Diseases, 100, 327–332. https://doi.org/10.1016/j.ijid.2020.09.016
-
Özdemir, Ö., Kasımoğlu, G., Bak, A., Sütlüoğlu, H., & Savaşan, S. (2024). Mast cell activation syndrome: An up-to-date review of literature. World Journal of Clinical Pediatrics, 13(2), 92813. https://dx.doi.org/10.5409/wjcp.v13.i2.92813
-
Alagheband, S., Cranford, C., & Stewart, P. (2019). Mast cell disorders and anaphylaxis. En M. Mahmoudi (Ed.), Allergy and asthma (pp. 1-33). Springer Nature Switzerland AG. https://doi.org/10.1007/978-3-319-58726-4_30-1
-
Peavy, R. D., & Metcalfe, D. D. (2008). Understanding the mechanisms of anaphylaxis. Current Opinion in Allergy and Clinical Immunology, 8(4), 310–315. https://doi.org/10.1097/ACI.0b013e3283036a90
-
Méndez-Enríquez, E., & Hallgren, J. (2019). Mast cells and their progenitors in allergic asthma. Frontiers in Immunology, 10, 821. https://doi.org/10.3389/fimmu.2019.00821
-
Jackson, C. W., Pratt, C. M., Rupprecht, C. P., Pattanaik, D., & Krishnaswamy, G. (2021). Mastocytosis and mast cell activation disorders: Clearing the air. *International Journal of Molecular Sciences*, *22*(20), 11270. https://doi.org/10.3390/ijms222011270
-
Afrin, L. B., Self, S., Menk, J., & Lazarchick, J. (2017). Characterization of Mast Cell Activation Syndrome. The American Journal of the Medical Sciences, 353(3), 207–215. https://doi.org/10.1016/j.amjms.2016.12.013
-
: Cardona, R., Muñoz-Ávila, M. A., Gómez-Henao, C., Diez-Zuluaga, S., & Gálvez-Cárdenas, K. M. (2019). Síndrome de activación mastocitaria. A propósito de un caso clínico. Revista Alergia México, 66(4), 504–509. https://doi.org/10.29262/ram.v66i4.587
-
Theoharides, T. C., Twahir, A., & Kempuraj, D. (2024). Mast cells in the autonomic nervous system and potential role in disorders with dysautonomia and neuroinflammation. Annals of Allergy, Asthma & Immunology: Official Publication of the American College of Allergy, Asthma, & Immunology, 132(4), 440–454. https://doi.org/10.1016/j.anai.2023.10.032
-
Mukai, K., Tsai, M., Saito, H., & Galli, S. J. (2018). Mast cells as sources of cytokines, chemokines and growth factors. Immunology Reviews, 282(1), 121–150. https://doi.org/10.1111/imr.12634
-
Albert-Bayo, M., Paracuellos, I., González-Castro, A. M., Rodríguez-Urrutia, A., Rodríguez-Lagunas, M. J., Alonso-Cotoner, C., Santos, J., & Vicario, M. (2019). Intestinal mucosal mast cells: key modulators of barrier function and homeostasis. Cells, 8(2), 135. https://doi.org/10.3390/cells8020135
-
Uranga, J. A., Martínez, V., & Abalo, R. (2020). Mast cell regulation and irritable bowel syndrome: Effects of food components with potential nutraceutical use. Molecules, 25(18), 4314. https://doi.org/10.3390/molecules25184314
-
Bischoff, S. C. (2016). Mast cells in gastrointestinal disorders. European Journal of Pharmacology, 778, 139–145. https://doi.org/10.1016/j.ejphar.2016.02.018
-
Cheng, L., Luo, Q. Q., & Chen, S. L. (2021). The role of intestinal mast cell infiltration in irritable bowel syndrome. Journal of Digestive Diseases, 22, 143–151. https://doi.org/10.1111/1751-2980.12971
-
González, M. I., Vannan, D. T., Eksteen, B., Flores-Sotelo, I., & Reyes, J. L. (2022). Mast cells in immune-mediated cholangitis and cholangiocarcinoma. Cells, 11(3), 375. https://doi.org/10.3390/cells11030375
-
Voelker, D., & Pongdee, T. (2025). Biomarkers in the diagnosis of mast cell activation. Current Opinion in Allergy and Clinical Immunology, 25(1), 27–33. https://doi.org/10.1097/ACI.0000000000001046
-
Beyens, M., Toscano, A., Ebo, D., Gülen, T., & Sabato, V. (2023). Diagnostic significance of tryptase for suspected mast cell disorders. Diagnostics, 13(24), 3662. https://doi.org/10.3390/diagnostics13243662
-
Valent, P., Hoermann, G., Bonadonna, P., Hartmann, K., Sperr, W. R., Broesby-Olsen, S., Brockow, K., Niedoszytko, M., Hermine, O., Chantran, Y., Butterfield, J. H., Greiner, G., Carter, M. C., Sabato, V., Radia, D. H., Siebenhaar, F., Triggiani, M., Gülen, T., Alvarez-Twose, I., ... Akin, C. (2023). The normal range of baseline tryptase should be 1 to 15 ng/mL and covers healthy individuals with HaT. Journal of Allergy and Clinical Immunology: In Practice, 11(10), 3010–3020. https://doi.org/10.1016/j.jaip.2023.08.008
-
Científico, N. (s/f). Nutricionista Científico. Nutricionista Científico. Recuperado el 20 de enero de 2026, de https://nutricionistacientifico.com/blog-details.php?id=13
-
Mehrani, Y., Morovati, S., Tieu, S., Karimi, N., Javadi, H., Vanderkamp, S., Sarmadi, S., Tajik, T., Kakish, J. E., Bridle, B. W., & Karimi, K. (2023). Vitamin D influences the activity of mast cells in allergic manifestations and potentiates their effector functions against pathogens. Cells , 12 (18), 2271. https://doi.org/10.3390/cells12182271
-
Calder, P. C. (2010). Omega-3 fatty acids and inflammatory processes. Nutrients, 2(3), 355–374. https://doi.org/10.3390/nu2030355
-
Maares, M., & Haase, H. (2016). Zinc and immunity: An essential interrelation. Archives of Biochemistry and Biophysics, 611, 58–65. https://doi.org/10.1016/j.abb.2016.03.022
-
Wessels, I., Fischer, H. J., & Rink, L. (2021). Dietary and physiological effects of zinc on the immune system. Annual Review of Nutrition, 41(1), 133–175. https://doi.org/10.1146/annurev-nutr-122019-120635
-
Nishida, K., & Uchida, R. (2018). Role of zinc signaling in the regulation of mast cell-, basophil-, and T cell-mediated allergic responses. Journal of Immunology Research, 2018, 5749120. https://doi.org/10.1155/2018/5749120
-
Marone, G., Columbo, M., de Paulis, A., Cirillo, R., Giugliano, R., & Condorelli, M. (1986). Physiological concentrations of zinc inhibit the release of histamine from human basophils and lung mast cells. Agents and Actions, 18(1–2), 103–106. https://doi.org/10.1007/bf01987995
-
Wan, Y., & Zhang, B. (2022). The impact of zinc and zinc homeostasis on the intestinal mucosal barrier and intestinal diseases. Biomolecules, 12(7), 900. https://doi.org/10.3390/biom12070900
-
Skrovanek, S., DiGuilio, K., Bailey, R., Huntington, W., Urbas, R., Mayilvaganan, B., Mercogliano, G., & Mullin, J. M. (2014). Zinc and gastrointestinal disease. World Journal of Gastrointestinal Pathophysiology, 5(4), 496–513. https://doi.org/10.4291/wjgp.v5.i4.496
-
Yao, Q., Zhang, W., Wang, Y., Shi, L., Zhao, Y., Liang, J., Zhao, Y., Kang, J., Zheng, X., Guo, R., Yuan, T., She, Y., & Liu, Z. (2025). Lactobacillus plantarum and galacto-oligosaccharides synbiotic relieve irritable bowel syndrome by reshaping gut Microbiota and attenuating mast cell hyperactivation. Nutrients, 17(10), 1670. https://doi.org/10.3390/nu17101670
-
Minutello, K., & Gupta, V. (2025). Cromolyn sodium. En StatPearls. StatPearls Publishing.
-
Cao, M., & Gao, Y. (2024). Mast cell stabilizers: from pathogenic roles to targeting therapies. Frontiers in Immunology, 15, 1418897. https://doi.org/10.3389/fimmu.2024.1418897
-
Weng, Z., Zhang, B., Asadi, S., Sismanopoulos, N., Butcher, A., Fu, X., Katsarou-Katsari, A., Antoniou, C., & Theoharides, T. C. (2012). Quercetin is more effective than cromolyn in blocking human mast cell cytokine release and inhibits contact dermatitis and photosensitivity in humans. PloS One, 7(3), e33805. https://doi.org/10.1371/journal.pone.0033805
-
Najaf Najafi, N., Armide, N., Akbari, A., Baradaran Rahimi, V., & Askari, V. R. (2024). Quercetin a promising functional food additive against allergic Diseases: A comprehensive and mechanistic review. Journal of Functional Foods, 116(106152), 106152. https://doi.org/10.1016/j.jff.2024.106152
-
Niijima-Yaoita, F., Tsuchiya, M., Ohtsu, H., Yanai, K., Sugawara, S., Endo, Y., & Tadano, T. (2012). Roles of histamine in exercise-induced fatigue: favouring endurance and protecting against exhaustion. Biological & Pharmaceutical Bulletin, 35(1), 91–97. https://doi.org/10.1248/bpb.35.91
-
Luttrell, M. J., & Halliwill, J. R. (2017). The intriguing role of histamine in exercise responses. Exercise and Sport Sciences Reviews, 45(1), 16–23. https://doi.org/10.1249/JES.0000000000000093
-
McCallion, A., Nasirzadeh, Y., Lingegowda, H., Miller, J. E., Khalaj, K., Ahn, S., Monsanto, S. P., Bidarimath, M., Sisnett, D. J., Craig, A. W., Young, S. L., Lessey, B. A., Koti, M., & Tayade, C. (2022). Estrogen mediates inflammatory role of mast cells in endometriosis pathophysiology. Frontiers in Immunology, 13, 961599. https://doi.org/10.3389/fimmu.2022.961599
-
Zierau, O., Zenclussen, A. C., & Jensen, F. (2012). Role of female sex hormones, estradiol and progesterone, in mast cell behavior. Frontiers in Immunology, 3, 169. https://doi.org/10.3389/fimmu.2012.00169
-
Shimbori, C., De Palma, G., Baer, L., Lu, J., Verdu, E. F., Reed, D. E., Vanner, S., Collins, S. M., & Bercik, P. (2022). Gut bacteria interact directly with colonic mast cells in a humanized mouse model of IBS. Gut Microbes, 14(1). https://doi.org/10.1080/19490976.2022.2105095
-
Lampiasi, N. (2022). Interactions between macrophages and mast cells in the female reproductive system. International Journal of Molecular Sciences, 23(10), 5414. https://doi.org/10.3390/ijms23105414
-
Xu, X., Wang, J., Guo, X., Chen, Y., Ding, S., Zou, G., Zhu, L., Li, T., & Zhang, X. (2023). GPR30-mediated non-classic estrogen pathway in mast cells participates in endometriosis pain via the production of FGF2. Frontiers in Immunology, 14, 1106771. https://doi.org/10.3389/fimmu.2023.1106771
-
Overman, E. L., Rivier, J. E., & Moeser, A. J. (2012). CRF induces intestinal epithelial barrier injury via the release of mast cell proteases and TNF-a. PLoS ONE, 7(6), e39935. https://doi.org/10.1371/journal.pone.0039935
-
Valent, P., Akin, C., Bonadonna, P., Hartmann, K., Brockow, K., Niedoszytko, M., Nedoszytko, B., Siebenhaar, F., Sperr, W. R., Oude Elberink, J. N. G., Butterfield, J. H., Alvarez-Twose, I., Sotlar, K., Reiter, A., Kluin-Nelemans, H. C., Hermine, O., Gotlib, J., Broesby-Olsen, S., Orfao, A., ... Metcalfe, D. D. (2019). Proposed Diagnostic Algorithm for Patients with Suspected Mast Cell Activation Syndrome (MCAS). The Journal of Allergy and Clinical Immunology: In Practice, 7(4), 1125–1133.e1. https://doi.org/10.1016/j.jaip.2019.01.006
-
Liu, Y., & Jiao, A. (2025). Flavonoids as immunoregulators: Molecular mechanisms in regulating immune cells and their therapeutic applications in inflammatory diseases. Frontiers in Immunology, 16, 1703672. https://doi.org/10.3389/fimmu.2025.1703672
-
Bodur, M., Yilmaz, B., Ağagündüz, D., & Ozogul, Y. (2025). Immunomodulatory effects of omega-3 fatty acids: Mechanistic insights and health implications. Molecular Nutrition & Food Research, 69(10), e202400752. https://doi.org/10.1002/mnfr.202400752
-
Murdaca, G., Allegra, A., Tonacci, A., Musolino, C., Ricciardi, L., & Gangemi, S. (2022). Mast cells and vitamin D status: A clinical and biological link in the onset of allergy and bone diseases. Biomedicines, 10(8), 1877. https://doi.org/10.3390/biomedicines10081877
-
Oksaharju, A., Kankainen, M., Kekkonen, R. A., Lindstedt, K. A., Kovanen, P. T., Korpela, R., & Miettinen, M. (2011). Probiotic Lactobacillus rhamnosus downregulates FCER1 and HRH4 expression in human mast cells. World Journal of Gastroenterology, 17(6), 750–759. http://dx.doi.org/10.3748/wjg.v17.i6.750
-
Forsythe, P., Wang, B., Khambati, I., & Kunze, W. A. (2012). Systemic effects of ingested Lactobacillus rhamnosus: Inhibition of mast cell membrane potassium (IKCa) current and degranulation. PLoS ONE, 7(7), e41234. https://doi.org/10.1371/journal.pone.0041234
-
Wang, Y., Tang, N., Mao, M., Zhou, Y., Wu, Y., Li, J., Zhang, W., Peng, C., Chen, X., & Li, J. (2021). Fine particulate matter (PM2.5) promotes IgE-mediated mast cell activation through ROS/Gadd45b/JNK axis. *Journal of Dermatological Science*, *102*(1), 47–57. https://doi.org/10.1016/j.jdermsci.2021.02.004