Conoce a tu sistema inmune, parte 4: Patologías autoinmunes, mecanismos comunes, causas y diferencias

La clave está en la ciencia, el cambio en ti
Sin duda alguna el sistema inmune es extremadamente complejo y su estudio da contenido em ha dado para crear fácilmente ya varios posts. Anteriormente ya he escrito 3 sobre sistema inmune (post 1,post 2,post 3).Hoy te presento la cuarta parte, las enfermedades autoinmunes.
Si viste mis anteriores publicaciones recordarás mi analogía del soldado, que representa a tus mastocitos, miembro del ejército del sistema inmune. En la tercera parte hice mención de cómo estos soldados se confunden y atacan sustancias inofensivas, generando alergias. En la enfermedad autoinmune ocurre esencialmente lo mismo, pero en vez de atacar un agente externo, el sistema inmune ataca componentes del mismo cuerpo (de ahí el prefijo “auto”, de auto ataque).
Condiciones en principio tan distintas como la artritis reumatoide, la diabetes tipo 1 o la esclerosis múltiple comparten un origen común. De hecho, se han identificado más de 100 enfermedades autoinmunes (Lista de enfermedades autoinmunes) en el ser humano, las cuales afectan hasta un 10% de la población en algunos países y aproximadamente 5% mundial (estudio,estudio).En este post nos enfocaremos en los mecanismos, causas, consecuencias y tratamientos de algunas patologías autoinmunes.
¿Qué es la autoinmunidad y qué funciones tiene el sistema inmune normalmente?
La enfermedad autoinmune es una patología en la cual el sistema inmune de una persona reacciona contra componentes propios del organismo, provocando daño en tejidos sanos. En condiciones normales, nuestro sistema inmune distingue entre lo propio de lo ajeno, protegiéndonos de infecciones y células anormales ( eliminando virus y bacterias invasoras, destruyendo células cancerígenas, y regulando la inflamación para reparar tejidos dañados). Mantiene una tolerancia inmune que evita atacar nuestras propias células o ataque sustancias o bacterias inofensivas. Cuando este equilibrio se rompe, el resultado puede ser la autoinmunidad: cuando el soldado que nos defiende nos ataca.
Los responsables de este ataque son los linfocitos T. En condiciones normales, el sistema inmune es capaz de filtrar los linfocitos T autorreactivos (los que nos atacan) y dejando pasar los demás linfocitos T reguladores (los que de verdad nos defienden) en un proceso llamado “Tolerancia central”. En caso de que algún linfocito autoreactivo se escape, existen mecanismos de tolerancia periférica que evitan que estos linfocitos T se salgan de control. La pérdida de tolerancia de este mecanismo da a luz la enfermedad autoinmune (estudio,estudio,estudio,estudio).

Enfermedades autoinmunes más conocidas
-
Diabetes tipo 1 (DM1): La diabetes tipo 1 se genera por la destrucción de las células β de los islotes de langerhans del páncreas que producen insulina. Esto provoca una pérdida progresiva de la capacidad de generación de insulina y, finalmente, a una deficiencia absoluta que provoca hiperglucemia crónica y cetoacidosis si no se administra la hormona de forma externa (estudio). Los pacientes con DM1 suelen debutar en infancia o adolescencia con sed excesiva, orina frecuente y pérdida de peso; requieren insulina de por vida para controlar su glicemia (estudio,estudio).
-
Artritis reumatoide (AR): La artritis reumatoide (AR) es una enfermedad que inflama múltiples articulaciones de forma simétrica y destrucción progresiva de cartílago y hueso, además del compromiso articular, puede presentar manifestaciones sistémicas, como nódulos subcutáneos, afectación pulmonar o vasculitis y que sin tratamiento, la AR puede evolucionar hacia deformidades articulares (estudio,estudio,estudio).
-
Lupus eritematoso sistémico (LES): Es una enfermedad en la que el sistema inmune fabrica anticuerpos contra el propio ADN y otras proteínas del núcleo. Cuando estos anticuerpos se unen a ese material, pueden acumularse en órganos como el riñón y generar inflamación; la nefritis lúpica es la complicación renal más frecuente. Los síntomas más comunes son; erupción malar, artralgias, fotosensibilidad, úlceras orales y la positividad de anticuerpos antinucleares (ANA >95% en series) facilitan el diagnóstico.(estudio,estudio,estudio,estudio,estudio)
-
Esclerosis múltiple (EM): Es una enfermedad del sistema nervioso central (cerebro y médula) en la que el propio sistema inmune ataca las vainas de mielina que ayudan a las neuronas a transmitir señales con rapidez. Ese ataque dificulta la transmisión nerviosa con síntomas que aparecen en forma de episodios (brotes) y que en muchos casos mejoran, pero que con el tiempo pueden dejar secuelas.Ejemplos de síntomas son visión borrosa por inflamación del nervio óptico, debilidad o parestesias en las extremidades, problemas de equilibrio, fatiga intensa entre otros.Suele comenzar en adultos jóvenes, y es más frecuente en mujeres (estudio,estudio)
-
Tiroiditis de Hashimoto: Consiste en la destrucción de la glándula tiroides. El sistema inmune ataca las células de la tiroides generando pérdida de función de la glándula. Hashimoto suele afectar más a mujeres de mediana edad. Sus síntomas son de hipotiroidismo: cansancio, aumento de peso, intolerancia al frío, caída de cabello, estreñimiento, entre otros. y suele encontrarse bocio (tiroides agrandada) al inicio, seguido de atrofia tiroidea en etapas tardías (estudio,estudio).
-
Psoriasis: En este caso el sistema inmunitario ataca la piel, haciendo que las células de la epidermis crezcan y se renueven muy rápido. Eso genera placas rojas, gruesas y escamosas que pican o duelen y suelen aparecer en áreas como cuero cabelludo, codos y rodillas (estudio,estudio).
Existen muchas patologías autoinmunes más que son interesantes (Gastritis autoinmune, enfermedad de Graves, addison), pero por temas de extensión no ahondaré mucho en ellas.
Causas del desequilibrio inmunológico en la autoinmunidad
La enfermedad autoinmune, como casi todas las enfermedades de hoy, es multifactorial, teniendo de base un factor común entre todas, concepto conocido como “tautología autoinmune”: las características en común superan sus diferencias, lo que explica por qué suelen coexistir varias condiciones autoinmunes en un mismo paciente o familia (estudio,estudio).
-
Susceptibilidad genética: La predisposición genética es un factor importante. Variantes en ciertos genes aumentan el riesgo de autoinmunidad. Ciertas versiones (alelos) de HLA predisponen fuertemente a enfermedades autoinmunes. Por ejemplo, los alelos HLA-DR3 y DR4 elevan el riesgo de diabetes tipo 1, y el HLA-DR15 se asocia a esclerosis múltiple (estudio,estudio,estudio,estudio). Es muy importante señalar que la genética no es determinante por sí sola sino como nuestros genes interactuan con el ambiente y como nuestros hábitos moldean la activación de estos (epigenética) (estudio).
-
Infecciones y mimetismo molecular: Infecciones (virus,bacterias) pueden gatillar la respuesta autoinmune mediante un mecanismo llamado mimetismo molecular. Ocurre cuando un patógeno contiene proteínas parecidas a componentes del cuerpo; al defendernos contra la infección, el sistema inmune “confunde” tejidos propios con el invasor debido a esas similitudes en su estructura (estudio). Un ejemplo clásico es la asociación del virus de Epstein-Barr con esclerosis múltiple: prácticamente todos los pacientes con EM tuvieron infección por EBV, y se ha observado que esta infección aumenta hasta 32 veces el riesgo de EM (estudio,estudio,estudio,estudio).

-
Microbiota intestinal e hipótesis de la higiene: La microbiota, el conjunto de microorganismos benéficos que habita principalmente en nuestro intestino, educa al sistema inmune en los primeros años de vida (investiga el concepto de los primeros 1000 dias). Una microbiota diversa promueve respuestas inmunes balanceadas. Alteraciones de la microbiota (disbiosis) se han vinculado con varias enfermedades autoinmunes (estudio). La hipótesis de la higiene postula que crecer en ambientes “demasiado limpios” o urbanos reduce la exposición normal a microorganismos en la infancia, lo que resulta en un sistema inmune mal entrenado que luego reacciona de forma exagerada contra alérgenos o tejidos propios (estudio). Distintos estudios apoyan esta idea: las enfermedades autoinmunes (y alérgicas) han aumentado en países más desarrollados en las últimas décadas en paralelo a la disminución de infecciones. Asimismo, vivir en zonas rurales (granjas, contacto con tierra y animales) parece otorgar cierta protección frente a autoinmunidad (como la EM), a diferencia del estilo de vida urbano (estudio,estudio). El tipo de parto también es importante dado que los niños que nacen de parto vaginal reciben una microbiota mas protectora y que los que nacen por cesárea. (estudio,estudio,estudio,estudio)

-
Factores hormonales y sexo: El 80% de los pacientes con enfermedades autoinmunes son mujeres, lo cual sugiere una fuerte influencia de las hormonas sexuales (Estrógenos y prolactina), más abundantes en mujeres, que influyen en el sistema inmune (estudio). Durante el embarazo (cuando los estrógenos están muy altos), algunas enfermedades autoinmunes como la artritis reumatoide suelen mejorar, mientras que otras como el lupus pueden exacerbar (estudio). Por otro lado, la testosterona ha mostrado tener efectos protectores.
-
Embarazo: Evidencias recientes sugieren que la etapa de gestación y las primeras instancias de la infancia (los “primeros 1000 días”) pueden influir en el riesgo de desarrollar patología autoinmune. Durante el embarazo, ocurre un intercambio de células entre madre y feto conocido como microquimerismo (fetal y maternal). Las células fetales pueden persistir en la madre y viceversa durante años (estudio). Se han hallado células maternas dentro de órganos de hijos con enfermedades autoinmunes, Inicialmente se planteaba que podrían actuar como desencadenantes: por ejemplo, en diabetes tipo 1, células transferidas de la madre al feto podrían infiltrar el páncreas del hijo y contribuir a la destrucción autoinmune de las células beta (estudio), pero este estudio plantea otra cosa. En su lugar, el aumento del microquimerismo sugiere que las células maternas detectan el daño en el páncreas y migran a esa zona buscando protegerlo. De igual modo, en lupus neonatal (un trastorno temporal en el bebé de madre con lupus), son autoanticuerpos maternos cruzando la placenta los que dañan tejidos del recién nacido. Además, condiciones maternas durante la gestación, como infecciones, deficiencias nutricionales o disbiosis en la microbiota de la madre – pueden influir en el desarrollo del sistema inmune fetal (estudio).
-
Estilo de vida y tóxicos ambientales: En la sociedad actual estamos expuestos a un gran número de tóxicos ambientales y que pueden contribuir a la enfermedad autoinmune, siendo el tabaquismo uno de los más importantes: los fumadores tienen riesgo mayor de artritis reumatoide (estudio,estudio) Otros tóxicos asociados son la sílice que se obtiene en mineria se asocia a lupus (estudio,estudio) y ciertos fármacos como la hidralazina y procainamida pueden causar un lupus medicamentoso). Por otra parte, la dieta, alta en ultraprocesados (azúcar, grasas industriales), se ha relacionado con más autoinmunidad (estudio) La obesidad también se ha asociado a mayor incidencia de enfermedades autoinmunes como de condiciones como artritis reumatoide o esclerosis múltiple, entre otras, pero no en todas ya que en el lupus no se encontró asociación (estudio).

-
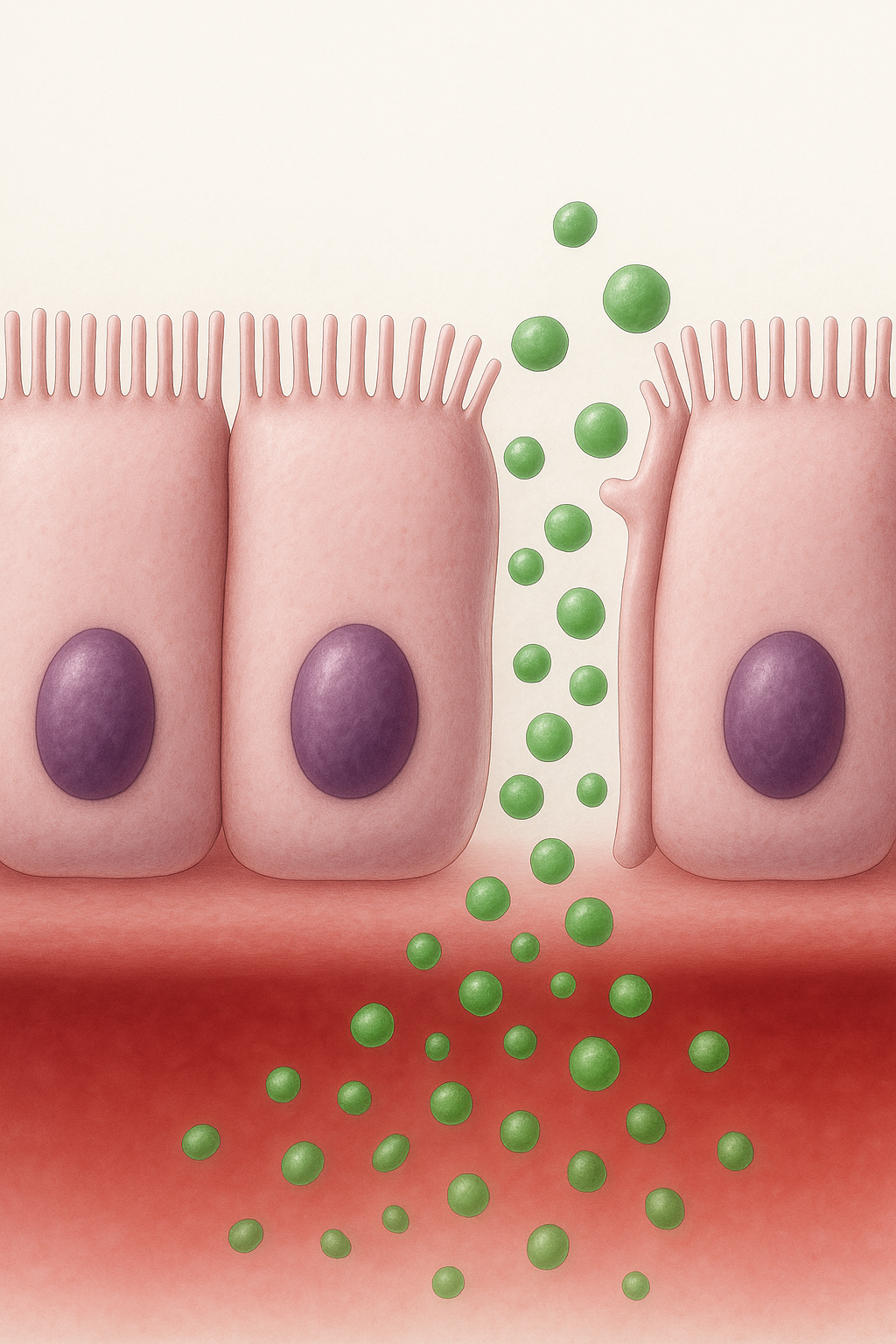
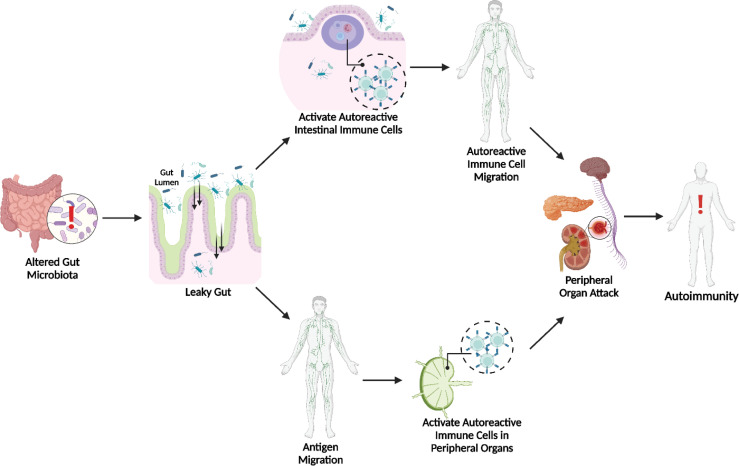
Leaky gut: Si viste mi post de leaky gut, recordarás que asocian aumento de la permeabilidad intestinal (“leaky gut”) con diversas enfermedades autoinmunes (p. ej. celiaquía, artritis reumatoide, enfermedad tiroidea autoinmune, EII) (estudio,estudio), pero la relación causal directa en humanos sigue en estudio y depende mucho del marcador usado (zonulina, test lactulosa/manitol, LPS, etc.) y de los mecanismos estudiados en cada patología (estudio,estudio,estudio). A modo de recordatorio, en el leaky gut lo que ocurre es que las uniones estrechas del intestino se abren y permiten paso de partículas, moléculas, bacterias o restos de comida (tras una infección, ingerir alimento contaminado o en mal estado) a la sangre y esto genera una activación del sistema inmune que en algunos casos puede generar reacción cruzada y terminar atacando a nuestro propio cuerpo.
Analítica y cómo se diagnostica/monitorea la autoinmunidad
El diagnóstico se puede separar en 2 categorías: Un perfil general y otro específico. ¿Por qué es así? Dado lo diverso de sus síntomas y que pueden afectar varios sistemas lo mejor es comenzar con un perfil general para tener una idea de que pruebas específicas podemos pedir (junto a los síntomas que presente el paciente) sin perder tiempo y dinero en pruebas que no vayan al caso.
PRUEBAS GENERALES
-
Hemograma completo (CBC):En las patologías crónicas y autoinmunes, es fundamental vigilar este parámetro de forma rutinaria. El objetivo es detectar a tiempo alteraciones en la sangre como la anemia (baja cantidad de glóbulos rojos), la leucopenia (disminución de las defensas o glóbulos blancos) o la trombocitopenia (bajo nivel de plaquetas).Estas alteraciones pueden aparecer por dos grandes motivos:
-
Por la propia enfermedad: La inflamación crónica prolongada, o alteraciones en el metabolismo que afectan la forma en que el cuerpo produce o destruye las células sanguíneas en la médula ósea.
-
Por el tratamiento: Muchos de los medicamentos necesarios para controlar enfermedades graves (como los inmunosupresores) tienen como efecto secundario alterar el trabajo de la médula ósea (estudio,estudio,estudio).
-
PCR (no es el test pcr, es proteína c reactiva): Se usa para medir inflamación general y cambia directamente en base a la inflamación presente, por lo que sube y baja rápidamente. Es sumamente útil para monitorizar si un tratamiento está funcionando en días o semanas, o para medir el estado inflamatorio general del cuerpo (aunque en pacientes con Lupus a veces no se eleva como debería o también no elevarse como debiera por algún fármaco) (estudio,estudio,estudio).
-
Perfil básico: hormonal, glucosa, perfil tiroideo TSH/T4,Hb1ac): Se solicitan en la evaluación inicial ante síntomas generales y luego sirven como marcadores de seguimiento en enfermedades autoinmunes endocrinas confirmadas (como tiroiditis de Hashimoto o diabetes mellitus tipo 1). No miden la inflamación, evalúan la función residual del órgano afectado Marcadores como el Péptido-C sirven para medir la reserva funcional y decidir el tipo de tratamiento (al revelar cuánta insulina propia sigue fabricando el páncreas en casos dudosos.Otros parámetros como la TSH o la Glucosa/HbA1c permiten un seguimiento rutinario para determinar las dosis de los tratamientos de reemplazo (levotiroxina o insulina) hasta restaurar el equilibrio perfecto del paciente (estudio,estudio,estudio,estudio,estudio).
-
Estudio de imagen (ecografía / Radiografía simple / Resonancia magnética): Confirma daño estructural del órgano; la modalidad a escoger depende de la composición del órgano a estudiar (ej. ecografía para evaluar tiroides, o resonancia magnética/ecografía para articulaciones) (estudio,estudio).
PRUEBAS ESPECÍFICAS
-
Autoanticuerpos: Hay distintos tipos de pruebas para buscarlos. Algunas sirven como primer filtro (cribado) y detectan muchos anticuerpos a la vez, como el ANA; otras buscan anticuerpos más específicos como ELISA; y en algunos casos se usan pruebas especiales que no sólo detectan el anticuerpo, sino que muestran si realmente hace algo en el cuerpo, por ejemplo estimular o bloquear una señal (bioensayos). El tipo de examen se elige según los síntomas y el contexto clínico, porque un resultado positivo por sí solo no siempre significa enfermedad (estudio,estudio,estudio).
-
Biopsia: Las biopsias (tomar un trocito de órgano) son la forma más directa de ver qué está ocurriendo: por ejemplo, en el riñón con lupus la biopsia dice exactamente qué tipo de lesión hay y eso determina qué tratamiento es necesario; en el hígado, una biopsia ayuda a diferenciar si el daño es por una enfermedad autoinmune (que necesita esteroides) o si es hígado graso (estudio,estudio).
Consecuencias de un sistema inmunológico desequilibrado (enfermedades autoinmunes)
Una vez generada la enfermedad autoinmunidad queda conocer algunas afecciones comunes. Algunas destacadas son:
-
Malabsorción o deficiencia de nutrientes: La malabsorción en enfermedades autoinmunes depende del órgano afectado, atrofia de la mucosa y vellosidades del intestino,, alteración de motilidad, déficit de enzimas/ bilis, ácido gástrico y del daño del órgano, acarreando deficiencias en nutrientes como hierro, b12, otros. Algunas enfermedades autoinmunes dañan las zonas del tubo digestivo encargadas de “absorber” vitaminas y minerales. Por ejemplo, la celiaquía destruye las vellosidades intestinales; la gastritis autoinmune impide que se forme el factor intrínseco, necesario para absorber la vitamina B₁₂; en crohn, la inflamación del íleon impiden la reabsorción de más nutrientes. Otras veces, los problemas con el movimiento intestinal permiten que crezcan bacterias donde no deben (SIBO) y éstas también evitan la correcta absorción (estudio,estudio,estudio,estudio).
-
Daño neurológico: Algunas enfermedades autoinmunes pueden afectar el sistema nervioso, aunque no todas con la misma frecuencia. En lupus, la cantidad de los pacientes que pueden presentar algún trastorno neuropsiquiátrico varía según la fuente dado que se consideran muchas patologías (las más graves no varían mucho pero la más sutiles si tienen diferencia según la fuente y el método de medición) (estudio,estudio). En Sjögren, los síntomas neurológicos son periféricos (afectan varias partes del cuerpo) y aparece en una cantidad pequeña pero importante de pacientes, aun así los resultados muestra gran variación según la fuente citada como se ve en este meta análisis (estudio).
-
Riesgo cardiovascular: Depende de la patología en gran medida. Por ejemplo la psoriasis aumenta el riesgo de evento cardiovascular en 46% en (estudio) Este impacto varía en otras condiciones: El Lupus incrementa el riesgo de desarrollar hipertensión arterial en un 240%, y el conjunto de patologías autoinmunes (la Artritis Reumatoide, el Lupus y el Síndrome de Sjögren) aumenta la presencia de placas ateroscleróticas en un 146% en comparación con la población sana (estudio).
Medidas de acción para mejorar el equilibrio inmunológico (prevención y manejo de autoinmunidad)
Como tal la enfermedad autoinmune no se cura, sino que se trata de cubrir lo que el cuerpo ya no puede hacer o enlentecer el avance de la patología. Adaptar la dieta a las dificultades que presente la patología en específico.Como dije antes,todas las enfermedades autoinmunes tienen una base común pero de ahí en adelante, en el tratamiento pueden haber muchas diferencias entre cada una ya sea en dieta o hábitos (DM1, sjogren, gastritis, hashimoto, entre otros).
-
Dieta: En primer lugar, la dieta debe respetar el contexto de cada enfermedad. Por ejemplo un paciente con diabetes 1 debe armar su dieta de modo de evitar picos de glucosa muy pronunciados (estudio), o un celíaco debe evitar el gluten y el contacto cruzado para evitar ingerir trazas de esta proteína (estudio). Cubierta esa base se debe pasar a la siguiente fase, la regulación inmunitaria y la inflamación mediante dieta. Determinados nutrientes son esenciales para una buena salud inmunitaria:
-
Zinc:Permite regular respuestas inmunes, alérgicas y estabilizar mastocitos y reparar la permeabilidad intestinal que puede exacerbar la respuesta inmune. (estudio,estudio,estudio).
-
Omega 3: La evidencia es mixta, los resultados no son igual de eficientes en cada caso. En artritis reumatoide hay beneficio en ensayos humanos, como reducción de dolor,(estudio) en lupus la muestran mejoría en algunos parámetros (a nivel cardiovascular pero no a nivel autoinmune) pero no en todos (estudio) y en esclerosis múltiple también hay señales favorables, pero basadas en pocos estudios (estudio). Además, una revisión reciente concluye que todavía hacen falta ensayos aleatorizados para validar con precisión la suplementación con omega-3 en prevención y manejo de autoinmunidad (estudio).
-
Vitamina D: Es más una hormona que una vitamina y sus niveles obtenibles a través de la dieta son escasos, siendo su mejor obtención a través del sol (o suplementación). Su rol más conocido es en la salud ósea, permitiendo, junto con el apoyo de magnesio y vitamina k, absorber calcio para tus huesos. La vitamina D también tiene un rol relevante en la respuesta inmune, al equilibrar la respuesta innata y adaptativa. La deficiencia de vitamina D se ha asociado con mayor incidencia de múltiples enfermedades autoinmunes. Su suplementación o generación via exposición al sol tiene un rol más preventivo, puesto que una vez instaurada la patología su efectividad en el tratamiento con vitamina D no ha mostrado resultados precisos, variando según la enfermedad autoinmune y el tipo de estudio y mostrando resultados interesante más a dosis altas y constantes, manteniendo niveles alto en sangre de forma permanente.Ten cuidado con el sol si tienes lupus: La radiación ultravioleta excesiva, se han vinculado a brotes de lupus cutáneo. (estudio,estudio,estudio,estudio,estudio,estudio).

-
Tratar la permeabilidad intestinal: Como mencioné más arriba, la permeabilidad intestinal está fuertemente asociada a distintas patologías autoinmunes. Para reparar las uniones estrechas te sugiero que evites alimentos desencadenantes (ultraprocesados, alcohol, alimentos a los que seas intolerante), controlar el estrés, sobretodo el crónico, consumir zinc (probado en reparar la barrera), la integración gradual de fibra (para no sobrecargar el intestino y favorecer la generación de ácidos grasos de cadena corta que alimentan las células y bacterias del intestino), y consumo de algunos probióticos (pero no cualquier cepa) son estrategias interesantes. (estudio,estudio,estudio).
-
Ejercicio físico regular (actividad moderada): El ejercicio no solo fortalece músculos y mejora la capacidad cardiovascular, sino que también ejerce un efecto antiinflamatorio e inmunomodulador cuando se practica de forma regular (estudio). Durante la actividad física, el músculo libera compuestos llamados mioquinas , que son antiinflamatorias (como IL-6 o IL-10) (estudio), Estudios en pacientes con artritis reumatoide, lupus y esclerosis múltiple han demostrado que programas de entrenamiento supervisado (ej. caminatas, bicicleta estática, natación, combinados con algo de ejercicio de resistencia) reducen marcadores inflamatorios como PCR o TNF-α e IL-6 (la IL- 6 es anti inflamatoria en ejercicio pero pro inflamatoria si viene de tejido adiposo) en comparación con pacientes sedentarios. Es importante individualizar: durante brotes muy activos de la enfermedad, puede que la tolerancia al ejercicio disminuya, por lo que se deben hacer ajustes (ejercicios de bajo impacto, estiramientos, fisioterapia). Pero incluso en esas fases, el movimiento ligero ayuda a evitar rigidez y mantener la función (estudio,estudio).
-
Manejo del estrés y salud mental: El estrés crónico psicológico (o físico) es un factor agravante de enfermedades autoinmunes. Hasta un 80% de pacientes refieren un evento estresante importante antes del inicio de su enfermedad o de un brote severo (estudio). ¿Por qué ocurre esto? El estrés sostenido altera el equilibrio del eje hipotálamo-hipófisis-suprarrenal (eje HPA), encargado de liberar cortisol, una hormona que en condiciones normales ayuda a limitar la inflamación. Bajo estrés constante, el organismo puede desarrollar una especie de “resistencia” al cortisol: los receptores ya no responden eficientemente y las glándulas pueden agotar su capacidad adaptativa (estudio). Por tanto, adoptar técnicas de manejo de estrés puede tener beneficios notorios: sal a caminar en la naturaleza, que ha mostrado reducir niveles de estrés, ten contacto social con seres queridos y realiza actividades que te traigan calma (ejercicio, películas,otros) (estudio,estudio).

-
Evitar el tabaco y alcohol: Dejar de fumar es una de las primeras recomendaciones en cualquier paciente autoinmune fumador – generalmente conduce a mejoras y puede reducir las exacerbaciones a largo plazo (estudio). En cuanto al alcohol, curiosamente un consumo moderado podría tener efectos protectores a diferencia de si es un consumo excesivo, pero las fuentes tiene problema de sesgo al tener cuestionarios (cifras oficiales pueden variar), sin embargo destacar que el seguimiento fue exhaustivo (estudio,estudio,estudio).
-
Cuidar la microbiota intestinal: La microbiota no solo educa al sistema inmune si no que participa de la misma respuesta inmunitaria. Una microbiota sana permite mejores respuestas a infecciones o reducir gravedad de la enfermedad autoinmune, incluso reducir incidencia. Para cuidar tu microbiota te sugiero
-
Consumir fibra:La fibra fermentable alimenta a las bacterias y favorece la producción de ácidos grasos de cadena corta, que ayudan a mantener saludable la barrera intestinal, a la regulación de la respuesta inmune, y reducir la inflamación (estudio,estudio,estudio).
-
Consumir fermentados: Los alimentos fermentados se consumen hace miles de años y en distintas partes del mundo. El queso, yogur, chucrut, kimchi, kombucha, kefir, son solo algunos ejemplos. Al principio se usaban para prolongar la vida útil de los alimentos, pero ahora se sabe que aportan multitud de beneficios (estudio) . Este estudio comprobó que una dieta alta en fermentados ,combinando hasta 6 porciones diarias entre de alimentos fermentados logró aumentar de forma constante la diversidad del microbioma y reducir hasta 19 marcadores inflamatorios en la sangre. Un consumo esporádico no basta, pero incluirlos diariamente como pilar de tu alimentación puede ayudar significativamente a calmar la hiperactividad del sistema inmune.
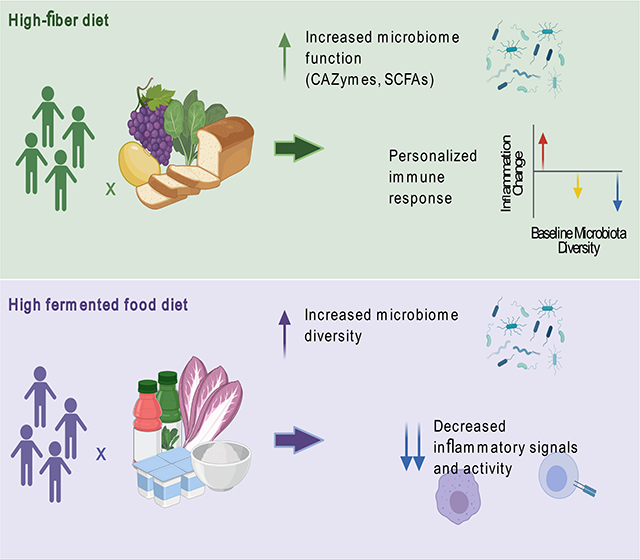
Fuente: Gut Microbiota-Targeted Diets Modulate Human Immune Status - PMC
-
Suplemento con probióticos: Una alternativa al consumo de fermentos es suplementarte con probióticos.Un estudio que evaluó a más de 7,400 niños con alto riesgo genético demostró que el consumo de probióticos en los primeros 27 días de vida redujo el riesgo de desarrollar DM1 hasta en un 60% en los más susceptibles genéticamente. ¿Por qué sucede esto? Esta revisión narrativa explica que ciertas cepas tienen efectos inmunomoduladores, fortaleciendo la barrera del intestino (evitando el intestino permeable) y reduciendo las señales de inflamación. Otro estudio observó que una dieta rica en fibra fermentable reduce riesgo de desarrollar DM1.
-
Trasplante fecal:Los trasplantes de microbiota fecal (TMF) ya se utilizan con éxito en colitis ulcerosa refractaria, y hay reportes de casos en esclerosis múltiple con resultados interesantes, aunque es una área emergente. Lo que se busca con este tratamiento es otorgarle a un paciente enfermo la microbiota de un paciente sano. Lo más probable es que un futuro no muy lejano incluso se puedan determinar perfiles compatibles entre donante y receptor con mucha mayor precisión, recibiendo la microbiota específica que uno necesite(estudio). Un caso interesante lo podemos ver en este estudio de caso de un paciente con esclerosis múltiple refractaria (resistente a fármacos) donde se detectaron mejoras en diversos síntomas tras tratamiento mantenido por 90 días de trasplante fecal mediante cápsulas.
-
Fármacos y terapias biológicas: Si bien el blog se enfoca en medidas de estilo de vida, no podemos dejar de mencionar la importancia de los fármacos en el manejo de las enfermedades autoinmunes ya establecidas. Los corticoides (ej. prednisona) reducen rápidamente la inflamación en brotes agudos, por otra parte, en casos crónicos se usan los FAMES (Fármacos Antirreumáticos Modificadores de Enfermedad o dmards por sus siglas en inglés).Los FAMEs convencionales (como el metotrexato) modulan la respuesta inmune a mediano plazo; y si no bastan, se avanza a los FAMEs biológicos (anticuerpos monoclonales), medicamentos de alta precisión que bloquean moléculas o células específicas (estudio,estudio,estudio).
Sugerencias finales
Convivir con una enfermedad autoinmune supone un desafío diario, pero la ciencia ha avanzado enormemente en la comprensión y tratamiento de estas patologías: hoy disponemos de terapias efectivas que han convertido condiciones antes incapacitantes en enfermedades manejables. Además, sabemos que nuestros propios hábitos pueden ser poderosos aliados. Recuerda la analogía del inicio: nuestro sistema inmune es como ese guardián confundido; mediante los cuidados adecuados, podemos ayudar a “reeducarlo” para que recupere su función protectora sin causar daño.