Conoce a tu sistema inmune, parte 3: Las alergias, conócelas y domínalas.
La clave está en la ciencia, el cambio está en ti
Vale, reconozco que me ha gustado mucho estudiar al sistema inmune y siento que a pesar de tener 2 partes previas (1,2), aún me quedan varios temas pendientes que son dignos de convertir en post. Por tal motivo he decidido traerles la tercera parte de este tema que me tiene tan enganchado. Sin más rodeos, te presento hoy las alergias.
Las alergias afectan hasta al 20-30% de la población (ligeras variaciones según sector)(3) y su frecuencia se estima irá en aumento, especialmente en niños y jóvenes (4).Seguramente conoces a alguien (o tú mismo) que no puede acercarse a un maní sin temer una reacción, o has visto bebés con dermatitis que luego desarrollan asma. Estas situaciones relativamente comunes harán que te preguntes: ¿por qué nuestro sistema inmune a veces sobrerreacciona a cosas inofensivas? ¿Es culpa de nuestros genes, del ambiente super limpio en que crecimos, o de la dieta moderna? Si leíste mi post anterior(2), recordarás mi analogía de los soldados. Estos soldados (los mastocitos), están entrenados para protegernos de invasores o actuar en daños internos (5,6). Su rol principal es protegernos, sin embargo en algunas ocasiones estos pierden el rumbo, se confunden y atacan a alimentos (leche, gluten, maní/cacahuete) o sustancias del ambiente (polen) generando variados síntomas en quien lo sufre (desde piel irritada, mocos, hasta diarreas severas, hemorragias o anafilaxia).
En este post conoceremos las alergias mediadas por IgE y no IgE, entendiendo sus mecanismos, causas (genéticas y ambientales), el rol del embarazo y los primeros años de vida, diferencias según entorno rural/urbano, sexo y cultura, y qué medidas (incluyendo dieta, suplementos y fármacos) se sugieren para manejarlas.
Sigamos conociendo este “ejército y sus soldados, los guardias inmunológicos” y sus posibles errores, con algunas analogías y evidencias científicas para guiarnos.
¿Qué son las alergias IgE y no IgE mediadas y qué función cumple la respuesta inmune?
Una alergia es, esencialmente, una reacción de hipersensibilidad iniciada por mecanismos inmunológicos frente a un antígeno (el que provoca la alergia) normalmente inofensivo. En otras palabras, el sistema inmunitario de la persona alérgica “confunde” sustancias ordinarias (como alimentos, ácaros y pólenes) con amenazas serias, desencadenando una respuesta defensiva exagerada que causa daño en el cuerpo (incluso en todos los sistemas) (7) .
Existen dos grandes tipos de alergias: las mediadas por IgE (inmunoglobulina E) y las no mediadas por IgE. Las alergias IgE-mediadas son las clásicas reacciones inmediatas (segundos o minutos después de la exposición) y son provocadas por anticuerpos IgE específicos que activan mastocitos y basófilos, liberando histamina y otros mediadores (7,8,9).
Por otro lado, las alergias no mediadas por IgE involucran otros componentes del sistema inmune (p. ej., linfocitos T, inmunidad innata) y suelen manifestarse de forma más tardía/demorosa (horas o días tras el contacto con el alérgeno) (10). Ejemplos de esto son ciertos trastornos gastrointestinales infantiles por algún alimento (FPIES) o la dermatitis de contacto por níquel (11) . Aunque sus mecanismos son distintos, ambos tipos de alergia comparten una base común: una desregulación o desequilibrio del sistema inmune.
Evolutivamente, en condiciones no patológicas, estas respuestas cumplen funciones específicas dentro del sistema inmune (12), participando en los siguientes roles clave:
-
Defensa antiparasitaria eficaz: La vía IgE evolucionó para protegernos de parásitos (ej. helmintos,lombrices intestinales, chagas, giardia, anisakis, etc) ) mediante liberación de histamina, contracciones musculares y secreciones que ayudan a expulsarlos. (12,13,14)
-
Mantenimiento de la tolerancia a alimentos y microbiota: En una persona sin alergia, el sistema inmune intestinal desarrolla tolerancia a las proteínas de los alimentos y a las bacterias que habitan en él. Esto implica respuestas que calman al sistema inmune ante exposiciones normales. Se ha propuesto que una microbiota diversa en la primera infancia educa al sistema inmune para que esta tolerancia pueda ser posible (15,16).
-
Reacción rápida contra venenos y alérgenos ambientales peligrosos: curiosamente, la reacción tipo alérgica también tiene cierta utilidad protectora en casos puntuales. Por ejemplo, la IgE puede inducir vómitos o diarrea frente a toxinas ingeridas, o estornudos y lagrimeo ante irritantes inhalados, actuando como un mecanismo rápido de expulsión. Este tipo de respuesta puede activarse frente a venenos verdaderos, como toxinas de serpientes, escorpiones o himenópteros (abejas y avispas), donde la reacción inmediata tiene una labor defensiva al limitar la carga tóxica.(13).
-
Memoria inmunológica exagerada: Tu sistema inmune recuerda al alérgeno. Esa memoria —sostenida por células plasmáticas que pueden producir IgE durante largos períodos y por células B memoria que pueden volver a originar IgE— permite que una persona sensibilizada reaccione hoy, mañana o años después. No obstante, que cada exposición sea más grave no es inevitable: depende de la afinidad de los anticuerpos, la cantidad de IgE en los mastocitos y el contexto inflamatorio (17).
Nota: Aunque las alergias mediadas por IgE se conocen mejor, las no-IgE son un grupo más diverso y menos estudiado. Ambas pueden usar los mismos “mensajeros” químicos (como las citoquinas IL-5 e IL-13) pero actúan por vías distintas y los síntomas pueden variar mucho entre personas (18,19).
Causas del desequilibrio que lleva a alergias (IgE y no IgE)
Las alergias no tienen un causante claro, único, o gran responsable, si no que es la suma de factores. Entre las principales causas o desencadenantes investigados se incluyen:
-
Carga genética y antecedentes familiares: La predisposición a la alergia tiene un importante componente hereditario (pero no determina). Tener padres alérgicos incrementa significativamente el riesgo de que un niño desarrolle alguna alergia,(20). Ejemplo de esto son variantes genéticas asociadas a atopia: por ejemplo, ciertas formas del HLA (Complejo Mayor de Histocompatibilidad) se vinculan con alergia al maní (20). Por otra parte las celulas TH2 (las responsables de la respuesta alérgica), tienen variantes específicas asociadas a la alergia, las TH2A (21,18).También puede ser la causa de que seas mas sensible genéticamente a algunos fármacos como AINES (22)
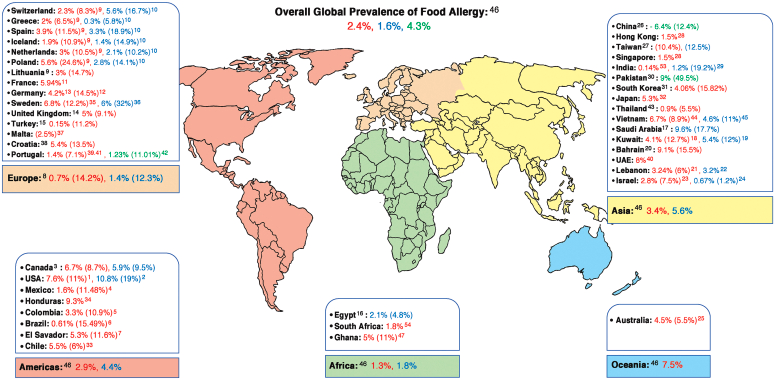
% de alergias segun sector. fuente: Feast for thought: A comprehensive review of food allergy 2021-2023 - PMC (20)
-
Ambiente ultra higiénico (Hipótesis de la higiene): Vivir en entornos demasiado limpios o con baja exposición a microorganismos en la infancia parece aumentar la susceptibilidad a alergias (te recomiendo estudies la llamada hipótesis de la higiene) Estudio mostró que niños criados en granjas o con muchos hermanos tenían menos alergias que niños urbanos con entornos muy higiénicos, viéndose resultados semejantes en distintos países (20,23). Por ejemplo se encontró que en Ciudad del Cabo (entorno urbano) la prevalencia de alergia alimentaria era 2.5%, mientras en áreas rurales de Sudáfrica era solo 0.5%(20) .
-
Primeros 1000 días de vida (embarazo y primeros 2 años): Este período – que abarca desde el nacimiento hasta aproximadamente los 2 años de edad – es fundamental para el “programar” el sistema inmune del infante. Las distintas circunstancias a las cuales esté expuesto en esta etapa dejan una huella que puede perdurar incluso toda la vida. Por ejemplo, la dieta materna y la salud durante el embarazo pueden aumentar o disminuir el riesgo de alergia del bebé, así como el tipo de parto: los bebés nacidos por cesárea (sin exposición a microbiota vaginal materna) muestran, en promedio, mayor propensión a reacciones alérgicas que los nacidos vía vaginal (24). Durante esta ventana crítica, también la introducción de alimentos y la colonización del intestino con bacterias beneficiosas calibran la respuesta inmune (48). Evidencias indican que alteraciones en la colonización normal (p.ej., por antibióticos tempranos o falta de lactancia materna) se asocian a mayor incidencia de alergias después (24,15).

-
Dieta occidental y microbiota alterada: Los cambios de hábitos en nuestra dieta y estilo de vida podrían estar impulsando la epidemia de alergias. Una dieta típica occidental, alta en ultraprocesados y baja en fibra, impacta negativamente la microbiota intestinal y promueve un estado proinflamatorio. Estudios señalan que el patrón alimentario occidental – pobre en fibra fermentable – reduce la producción de ácidos grasos de cadena corta en el intestino (estos ácidos grasos efecto antiinflamatorio y promotor de tolerancia inmune) (25). La menor ingesta de fibra y antioxidantes, junto con mayor consumo de Omega-6 respecto a Omega-3, se ha relacionado con aumento de enfermedades alérgicas y asmáticas (26). En cambio, dietas ricas en frutas, vegetales y pescado (como la mediterránea) podrían tener un efecto protector modulando la inmunidad.
-
Sexo y hormonas: Curiosamente, el riesgo de alergia varía según el sexo y la etapa de la vida. En la infancia, los varones tienden a presentar alergias (asma, eczema, alergias alimentarias) con mayor frecuencia que las mujeres. Sin embargo, después de la pubertad esta relación se invierte en varias condiciones – por ejemplo, el asma y la rinitis alérgica se reportan más en mujeres jóvenes adultas (27). Las hormonas sexuales parecen influir en la respuesta inmune alérgica: el estrógeno potencia las respuestas de tipo Th2 (promoviendo más IgE, mayor activación de mastocitos), mientras que hormonas como la progesterona y los andrógenos tienden a atenuar la reacción alérgica. Esto podría explicar por qué, tras la adolescencia, las mujeres – con niveles altos de estrógenos cíclicos – muestran mayor predisposición a algunas alergias y a cuadros más graves (por ejemplo, exacerbaciones asmáticas ligadas al ciclo menstrual en ciertas pacientes).
-
Infección por parásitos (Anisakis spp.): La exposición a Anisakis a través del consumo de pescado crudo o insuficientemente cocido puede inducir una respuesta inmune con producción de IgE específica frente a antígenos del parásito. Esto no solo explica los cuadros de anisakiasis gastrointestinal, sino también manifestaciones alérgicas inmediatas (urticaria, angioedema o anafilaxia) tras la ingesta de pescado contaminado. Esta reacción puede quedar como secuela y haber reacción alérgica al comer pescado por trazas de anisakis (aunque esté cocido el pescado y el parásito muerto). (28,29)
- Intestino permeable o leaky gut: El intestino permeable es una causa y consecuencia las alergías. En el leaky gut/intestino permeable las uniones estrechas del intestino se abren y permiten entrada de restos alimentos a la sangre facilitando la respuesta alérgica, y a su vez, al ocurrir una respuesta alérgica, esta aumenta la permeabilidad del intestino en un ciclo vicioso (64,65) Hace un tiempo hice un post de leaky gut, te invito a leerlo (66).
- Dermatitis atópica (eccema): La dermatitis atópica es una enfermedad crónica de la piel con pérdida de la barrera cutánea (p. ej. mutaciones en filagrina) que facilita la entrada de alérgenos y bacterias. Los lactantes con dermatitis atópica moderada-grave presentan mayor probabilidad de alergia alimentaria y, con el tiempo, de evolucionar hacia asma o rinitis (la llamada «marcha atópica») (33).
Consecuencias de una respuesta alérgica desequilibrada
Una vez perdido el equilibrio y la alergia ya se genera queda explicar los distintos tipos de reacciones alérgicas y sus consecuencias.
-
Anafilaxia: Es la manifestación más extrema y peligrosa de una alergia. Se trata de una reacción sistémica (afecta a todo el cuerpo) que ocurre de forma rápida y puede ser mortal de no tratarse. En la anafilaxia se da lugar a una liberación masiva de mediadores —como histamina y leucotrienos— que provoca síntomas que incluyen vasodilatación, cierre de vías respiratorias, hipotensión, mareos, cierre de garganta, taquicardia, entre otros.Se trata con epinefrina (30).
-
Asma alérgica: Una respuesta alérgica desequilibrada en las vías respiratorias puede evolucionar a asma, caracterizado por inflamación crónica de los bronquios, hiperreactividad y obstrucción variable del flujo aéreo. Aproximadamente la mitad de los casos de asma tienen un componente alérgico (desencadenado por alérgenos como ácaros, pólenes, caspa de animales)(6,31,32).
-
Rinitis alérgica y sinusitis crónica: Los síntomas de la rinitis alérgica son estornudos, congestión, picor nasal, lagrimeo. También puede perjudicar el sueño y coexistir con asma si no se le toma enserio y, cuando es persistente, puede asociarse a sinusitis crónica y pólipos en algunos casos (32).
-
Alergia alimentaria y trastornos digestivos: La pérdida de tolerancia oral a ciertos alimentos puede llevar a alergias alimentarias. Las alergias alimentarias pueden provocar desde urticaria y vómitos hasta anafilaxia con apenas trazas del alimento. Niños con múltiples alergias alimentarias presentan con mayor frecuencia déficits nutricionales y retrasos en el crecimiento, debido a las dietas de exclusión necesarias o a los síntomas digestivos que genera la reacción alérgica (11,34).
-
Esofagitis eosinofílica: La esofagitis eosinofílica (EoE) es una enfermedad crónica del esófago causada por la acumulación de un tipo de glóbulos blancos (eosinófilos) en respuesta a alérgenos como alimentos, polen, otros. Los síntomas incluyen:disfagia, hemorragias, dolor torácico, vómitos, reflujo, pérdida de peso o mala ganancia en casos crónicos. Como tal no es una alergia pura, sino mixta (IgE y no IgE mediada). Se Diagnóstica con endoscopia con biopsias que muestran ≥15 eosinófilos/HPF y exclusión de otras causas (35).
-
Carga socioeconómica y emocional: Las alergias crónicas incrementan costos sanitarios y ausencia laboral de los padres y por parte del escolar en casos de crisis generan alta carga emocional (especialmente en cuidadores de niños con alergia alimentaria) y dificultan la vida social del afectado a la hora por ejemplo, comer afuera o salir de fiesta(34).
Analítica y diagnóstico de las alergias
¿Cómo se diagnostica una alergia? Dado que muchos síntomas se asemejan a otras condiciones, el diagnóstico se apoya en una combinación de historia clínica detallada y pruebas específicas de laboratorio o piel (36).
Si sospechas que tienes alguna alergia te dejo los principales biomarcadores y pruebas diagnósticas empleadas, junto con su interpretación y limitaciones:
1) Inmunoglobulina E total en suero: mide la cantidad total de anticuerpos IgE circulantes en sangre. Suele estar elevada en personas atópicas (con múltiples alergias, eczema, etc.),(37,38).
-
¿Cuándo pedirla? Cuando se sospecha fuertemente atopia sistémica (p. ej., un niño con eczema difuso y asma) como dato orientativo.
-
Interpretación: niveles altos apoyan una base atópica, pero ojo: niveles normales de IgE no excluyen alergias, especialmente alergias limitadas a uno o pocos alérgenos. Además, una IgE total alta tampoco identifica qué causa la alergia – se necesita pruebas más específicas.
2) IgE específica (pruebas en sangre de alérgenos individuales): Esta prueba detecta anticuerpos IgE dirigidos a un alérgeno concreto (p. ej. maní, ácaro) (39).
-
¿Cuándo pedirla? Pídela cuando la historia clínica sugiera una reacción ligada a ese alimento/causa – por ejemplo, urticaria y dificultad respiratoria tras comer huevo
-
Interpretación: un resultado positivo confirma sensibilización, pero no equivale automáticamente a alergia clínica sin coherencia temporal/compatible (puede existir sensibilidad cruzada)
3) Pruebas cutáneas (skin-prick test): Esta prueba detecta sensibilización IgE in vivo: se coloca el extracto del posible alergeno sobre la piel (polen, ácaros, alimentos) y se realiza una punción en la piel; si hay IgE fijada a mastocitos aparece un habón (roncha elevada + enrojecimiento). en aproximadamente 15 minutos.(40,41).
-
¿Cuándo realizarlas? Son de primera línea en la evaluación de alergias inmediatas a aeroalergenos (rinitis, asma alérgica) y alimentos, porque son rápidas, sensibles y de bajo costo. Un prick test positivo (habón ≥3 mm mayor al control) indica sensibilización IgE in vivo.
-
Interpretación: Al igual que con IgE en sangre, tiene alta sensibilidad y buen valor predictivo negativo – un prick negativo prácticamente descarta alergia IgE a esa sustancia, pero su valor predictivo positivo es bajo si no hay sospechas en base a los síntomas clínicos. Es decir, un habón positivo significa presencia de IgE, pero podríamos sobre-diagnosticar alergias si testeamos “a ciegas”.
4)Pruebas de parche (patch test): Las pruebas de parche (patch test) son la herramienta estándar para diagnosticar dermatitis de contacto (hipersensibilidad retardada tipo IV). Se aplican parches en la espalda durante ~48 horas y se realizan lecturas tempranas y tardías (48 h y 72–96 h) (42).
¿Cuándo se usan? Para sospecha de dermatitis de contacto alérgica (por metales como níquel, fragancias, químicos industriales, etc.) o en evaluación de alergias alimentarias retardadas (p.ej., algunos casos de esofagitis eosinofílica o proctocolitis alérgica del lactante).
-
Interpretación: Un parche positivo se manifiesta como enrojecimiento, pápulas o vesículas en el sitio del alérgeno, indicando hipersensibilidad. Es muy útil para identificar causantes de eczemas crónicos de contacto.
-
Limitaciones: No hay alérgenos de parche disponibles o validados para todos los posibles causantes; en alergia alimentaria no IgE (como esofagitis eosinofílica) los tests de parche y prick tienen baja correlación con los desencadenantes reales y no se consideran suficientemente fiables para guiar la dieta. Un ejemplo: un paciente con sospecha de EoE puede tener parches negativos a leche/trigo pero aún así esos alimentos ser causantes – la única forma de confirmarlo sería con dieta de eliminación y reintroducción controlada (63).
5)Pruebas de provocación (desencadenamiento controlado): Consisten en exponer al paciente al alérgeno sospechoso de manera controlada y escalonada, observando si presenta reacción. Pueden ser provocaciones orales alimentarias (dar el alimento en dosis crecientes bajo supervisión médica) o provocaciones inhalatorias (ej. prueba bronquial con alérgeno en investigación, ej: polen) (36).
-
¿Cuándo se indican? Son el estándar de oro para diagnosticar alergia alimentaria cuando la historia y las pruebas no son concluyentes. Por ejemplo, si un niño tiene IgE específica baja y prick dudoso al huevo, pero nunca lo ha comido, una provocación oral controlada confirmará si realmente es alérgico o puede tolerarlo. También se usan para evaluar tolerancia adquirida (ver si una alergia se resolvió).
-
Interpretación: Un resultado positivo (aparición de síntomas objetivos durante la prueba) confirma la alergia clínica. Un resultado negativo (ninguna reacción hasta dosis completa) indica que el alimento es tolerado.
Medidas de acción para mejorar o manejar las alergias
Si bien la genética no la podemos cambiar, muchos de los factores ambientales y de estilo de vida que influyen en las alergias sí son modificables. Además, hoy contamos con estrategias efectivas para mitigar las manifestaciones alérgicas e incluso inducir tolerancia en algunos casos.
-
Lactancia materna exclusiva primeros 6 meses, ideal 2 años: Esta es una recomendación universal que también muestra beneficios en la alergia. La leche materna aporta Inmunoglobulinas protectoras como la IgA (39), sustancias antiinflamatorias, probióticos y prebióticos que promueven una microbiota saludable y educan al sistema inmune del bebé (43). Estudios sugieren que los bebés amamantados tienen menor incidencia de eccema,asma y rinitis en la infancia (44) . Si la alergia ya se manifestó no es necesario suspender la leche materna (pero la madre si debe suspender consumo de lácteos), sin embargo, si por alguna razón no puedes darle leche o se te dificulta y debes darle un apoyo o reemplazo,prueba con fórmulas lácteas extensamente hidrolizadas. son muy seguras, aunque no son de sabor muy agradable que digamos (45). Te dejo una fundación especialista en alergias con su tienda (46,62).
-
Evitar el tabaco: Estudios han mostrado que exponerse al humo del tabaco (en especial cuando es en distintos entornos (casa, trabajo, escuela, etc) aumenta rl riesgo de alergias como asma (47). En mujeres embarazadas aumenta el riesgo de asma en el feto (48).
-
Introducción temprana y vigilada de alimentos alergénicos: Contrario a viejas creencias de retrasar alimentos “peligrosos”, la evidencia reciente indica que introducir ciertos alérgenos alimentarios durante la lactancia o alrededor de los 6 meses puede reducir el riesgo de alergia. Un ejemplo es el caso del maní: este ensayo clínico demostró que bebés con alto riesgo que consumieron cacahuete regularmente desde los 4–11 meses tuvieron hasta un 86% menos de alergia al maní a los 5 años, comparado con aquellos que lo evitaron (49).
-
Ensuciate: Vale, no digo que no te bañes nunca más o que no te laves la manos, ya que si es necesaria una higiene mínima, pero también permite que tu hijo juegue en el parque, se manche con barro, interactúe con niños en el jardín de niños y convivir con mascotas y no abusar de antibióticos permitirá entrenar a tu sistema inmune de manera eficaz y entretenida (23). En cuanto a las embarazadas pasar tiempo en entornos verdes o de granja podría influir positivamente en la microbiota que transmitirán al bebé.(23)
-
Comer comida real: Aumentar consumo de fibra fermentable (soluble,en semillas como Chia, frutas, verdurass) en la medida que la toleres ayudará para mejorar la composición de tu microbiota y producir SCFA (ácido grasos de cadena corta) que, según revisiones, pueden atenuar la activación de mastocitos al tener efecto anti inflamatorio(26).
-
Suplementos probióticos y salud intestinal: Dado el papel de la microbiota en el sistema inmune, se han estudiado los probióticos como estrategia para prevenir o tratar alergias. Un metaanálisis de 29 ensayos clínicos (50) muestra una reducción modesta del riesgo de dermatitis atópica cuando probióticos se administran en el periodo perinatal o al lactante, pero la certeza de la evidencia no es muy alta que digamos (hay mucha variabilidad de resultados) y los efectos dependen fuertemente de la cepa, el momento y la dosis. No hay pruebas consistentes de prevención de asma u otras alergias. Si se consideran, deben recomendarse de forma específica (cepa/dosis) y con asesoría clínica. Ojo, no digo que no sirvan pero hay que ver caso a caso (16).
-
Suplementación con Quercetina: Un estudio reciente destaca que este antioxidante (presente en cebollas y manzanas) actúa estabilizando los mastocitos para que no liberen histamina y reduciendo la producción de IgE, ayudando a controlar síntomas (51)
-
Vitamina D: La vitamina D ayuda a regular la respuesta inmune y estabilizar los mastocitos. Procura tener unos 40 ng/dl como mínimo. Con dosis de 2000-5000 UI/d irás bien (52,53).
-
Omega 3: El omega 3 ha mostrado efectos interesantes en el asma en embarazo,pero no se puede decir lo mismo para el eccema, donde no hay efectos. Por otra parte en alergias alimentarias los resultados aún no son definitivos (falta claridad) (54). De todas formas el omega 3, tiene efectos que van más allá de prevenir alergias y puede ser útil de otras maneras (55).
-
Fármacos: Se emplean antihistamínicos y corticosteroides tópicos generalmente (56).
-
Evitar desencadenantes: suena obvio, pero es un pilar. Por ejemplo, en alérgicos a ácaros, usar fundas antiácaros en almohada/colchón, lavar sábanas y reducir humedad ambiental ayuda a disminuir la carga alergénica en el dormitorio. Usar purificadores de aire con filtro HEPA (57,58).
-
Contacto cruzado:Ten mucho cuidado con la contacto cruzado, a veces mirada en menos, pero puede ser el gatillante de muchas reacciones si no eres cuidadoso. Las pequeñas trazas que quedan en la comida, a veces con mero contacto, pueden generar reacción. A modo de ejemplo si tuvieses alergía a la proteína de la leche de vaca y cortó un trozo de queso con un cuchillo y luego tu usas ese cuchillo ya podrías reaccionar (59,60).
-
Terapias biológicas y emergentes: Para casos de alergias severas refractarias (resistente a tratamiento), existen medicamentos conocidos como anticuerpos monoclonales que bloquean pasos clave de la reacción alérgica. Un ejemplo es omalizumab, un anti-IgE que se une a IgE libres impidiendo su fijación a receptores y que activen mastocitos – se usa en asma alérgica grave y urticaria crónica espontánea con buenos resultados, reduciendo síntomas[xx.)Otros biológicos dirigidos a IL-5/IL-5R, IL-4R (dupilumab) o TSLP (tezepelumab) muestran eficacia en fenotipos específicos de asma y en dermatitis atópica, ampliando opciones para pacientes severos. .y recientemente las guías europeas sugieren su uso en alergia alimentaria mediada por IgE (31,38,61).

Sugerencias finales
Las alergias IgE y no IgE no son aleatorias. Detrás de un niño alérgico suele coexistir una predisposición genética y un entorno moderno con escaso entrenamiento del sistema inmune que termina gatillando estas patologías. En muchos casos, patologías del adulto como el asma pueden rastrearse a manifestaciones tempranas —por ejemplo, dermatitis atópica— siguiendo la marcha atópica.
La evidencia y la práctica clínica son firmes en algo: equilibrio y adaptación a cada caso. No se trata de ambientes insalubres ni de una esterilidad extrema, sino de exposiciones adecuadas y progresivas a bacterias, alimentos y naturaleza en ventanas críticas del desarrollo. Realizado de manera correcta se generan efectos duraderos y, incluso aunque se manifieste una alergia, hoy en día existen múltiples recursos para tratarlas.

Referencias
-
Científico, N. (s. f.). Nutricionista Científico | Nutrición basada en ciencia. Nutricionista Científico. https://nutricionistacientifico.com/blog-details.php?id=15
-
Científico, N. (s. f.-b). Nutricionista Científico | Nutrición basada en ciencia. Nutricionista Científico. https://nutricionistacientifico.com/blog-details.php?id=19
-
Alska, E., Doligalska, A., Napiórkowska-Baran, K., Dolina, M., Osińska, K., Pilichowicz, A., Wojtkiewicz, A., Kaczor, J. J., Szymczak, B., & Bartuzi, Z. (2025). Global Burden of Allergies: Mechanisms of Development, Challenges in Diagnosis, and Treatment. Life, 15(6), 878. https://doi.org/10.3390/life15060878
-
De los Andes, C. U. (s. f.). Alergias: el año 2050 más de la mitad de la población padecería alguna. Uandes. https://www.clinicauandes.cl/noticia/aumento-de-alergias-el-anno-2050-mas-de-la-mitad-de-la-poblaci%C3%B3n-padeceria-alguna
-
Galván-Morales, M. Á., Vizuet-de-Rueda, J. C., Montero-Vargas, J. M., & Teran, L. M. (2025). Role of Mast Cells in Human Health and Disease: Controversies and Novel Therapies. International Journal of Molecular Sciences, 26(18), 8895. https://doi.org/10.3390/ijms26188895
-
Banafea, G. H., Bakhashab, S., Alshaibi, H. F., Pushparaj, P. N., & Rasool, M. (2022). The role of human mast cells in allergy and asthma. Bioengineered, 13(3), 7049-7064. https://doi.org/10.1080/21655979.2022.2044278
-
Bellanti, J. A. (2024). IgE and non-IgE food allergy: A review of immunological mechanisms. Journal of Food Allergy, 6, 37–46. https://doi.org/10.2500/jfa.2024.6.240003
-
González-de-Olano, D., & Álvarez-Twose, I. (2018). Mast cells as key players in allergy and inflammation. Journal of Investigational Allergology and Clinical Immunology, 28(6), 365–378. https://doi.org/10.18176/jiaci.0327
-
Pundit, V. A., Makkoukdji, N., Banegas-Carballo, K. M., Stone, F., Satnarine, T., Kuhn, J., Kleiner, G. I., & Gans, M. D. (2024). A review of non-IgE immune-mediated allergic disorders of the gastrointestinal tract. Gastrointestinal Disorders, 6(2), 478–496. https://doi.org/10.3390/gidisord6020033
-
Zhang, S., Sicherer, S., Berin, M. C., & Agyemang, A. (2021). Pathophysiology of Non-IgE-Mediated Food Allergy. ImmunoTargets and Therapy, 10, 431-446. https://doi.org/10.2147/ITT.S284821
-
Nowak-Węgrzyn, A., Chehade, M., Groetch, M. E., Spergel, J. M., Wood, R. A., Allen, K., Atkins, D., Bahna, S., Barad, A. V., Berin, C., Whitehorn, T. B., Burks, A. W., Caubet, J., Cianferoni, A., Conte, M., Davis, C., Fiocchi, A., Grimshaw, K., Gupta, R., . . . Greenhawt, M. (2017). International consensus guidelines for the diagnosis and management of food protein–induced enterocolitis syndrome: Executive summary—Workgroup Report of the Adverse Reactions to Foods Committee, American Academy of Allergy, Asthma & Immunology. Journal Of Allergy And Clinical Immunology, 139(4), 1111-1126.e4. https://doi.org/10.1016/j.jaci.2016.12.966
-
Hellman, L. T., Akula, S., Thorpe, M., & Fu, Z. (2017). Tracing the Origins of IgE, Mast Cells, and Allergies by Studies of Wild Animals. Frontiers In Immunology, 8, 1749. https://doi.org/10.3389/fimmu.2017.01749
-
Mukai, K., Tsai, M., Starkl, P., Marichal, T., & Galli, S. J. (2016). IgE and mast cells in host defense against parasites and venoms. Seminars in Immunopathology, 38(5), 581–603. https://doi.org/10.1007/s00281-016-0565-1
-
Pritchard, D. I., Falcone, F. H., & Mitchell, P. D. (2021). The evolution of IgE-mediated type I hypersensitivity and its immunological value. Allergy, 76(4), 1024–1040. https://doi.org/10.1111/all.14570
-
Ismail, I. H., Oppedisano, F., Joseph, S. J., Boyle, R. J., Licciardi, P. V., Robins-Browne, R. M., & Tang, M. L. K. (2012). Reduced gut microbial diversity in early life is associated with later development of eczema but not atopy in high-risk infants. Pediatric Allergy and Immunology, 23(7), 674–681. https://doi.org/10.1111/j.1399-3038.2012.01328.x
-
Mares, R. C., Săsăran, M. O., & Mărginean, C. O. (2025). Gut Microbiota and Food Allergy: A Review of Mechanisms and Microbiota-Targeted Interventions. Nutrients, 17(18), 3009. https://doi.org/10.3390/nu17183009
-
Satitsuksanoa, P., Daanje, M., Akdis, M., Boyd, S. D., & Van de Veen, W. (2020). Biology and dynamics of B cells in the context of IgE‐mediated food allergy. Allergy, 76(6), 1707-1717. https://doi.org/10.1111/all.14684
-
Huang, Z., Chu, M., Chen, X., Wang, Z., Jiang, L., Ma, Y., & Wang, Y. (2022). Th2A cells: The pathogenic players in allergic diseases. Frontiers in Immunology, 13, 916778. https://doi.org/10.3389/fimmu.2022.916778
-
Kumar, M., Duraisamy, K., & Chow, B. (2021). Unlocking the Non-IgE-Mediated Pseudo-Allergic Reaction Puzzle with Mas-Related G-Protein Coupled Receptor Member X2 (MRGPRX2). Cells, 10(5), 1033. https://doi.org/10.3390/cells10051033
-
Bartha, I., Almulhem, N., & Santos, A. F. (2024). Feast for thought: A comprehensive review of food allergy 2021-2023. Journal of Allergy and Clinical Immunology, 153(3), 576-594. https://doi.org/10.1016/j.jaci.2023.11.918
-
Wambre, E., Bajzik, V., DeLong, J. H., O’Brien, K., Nguyen, Q., Speake, C., Gersuk, V. H., DeBerg, H. A., Whalen, E., Ni, C., Farrington, M., Jeong, D., Robinson, D., Linsley, P. S., Vickery, B. P., & Kwok, W. W. (2017). A phenotypically and functionally distinct human T H 2 cell subpopulation is associated with allergic disorders. Science Translational Medicine, 9(401). https://doi.org/10.1126/scitranslmed.aam9171
-
Amo, G., Cornejo-García, J. A., García-Menaya, J. M., Cordobes, C., Torres, M. J., Esguevillas, G., ... & García-Martín, E. (2016). FCERI and histamine metabolism gene variability in selective responders to NSAIDS. Frontiers in Pharmacology, 7, 353. https://doi.org/10.3389/fphar.2016.00353
-
Pfefferle, P. I., Keber, C. U., Cohen, R. M., & Garn, H. (2021). The hygiene hypothesis – learning from but not living in the past. Frontiers in Immunology, 12, 635935. https://doi.org/10.3389/fimmu.2021.635935
-
Davis, E. C., Monaco, C. L., Insel, R., & Järvinen, K. M. (2024). Gut microbiome in the first 1000 days and risk for childhood food allergy. Annals Of Allergy Asthma & Immunology, 133(3), 252-261. https://doi.org/10.1016/j.anai.2024.03.010
-
Agus, A., Denizot, J., Thévenot, J., Martinez-Medina, M., Massier, S., Sauvanet, P., Bernalier-Donadille, A., Denis, S., Hofman, P., Bonnet, R., Billard, E., & Barnich, N. (2016). Western diet induces a shift in microbiota composition enhancing susceptibility to Adherent-Invasive E. coli infection and intestinal inflammation. Scientific Reports, 6, 19032. https://doi.org/10.1038/srep19032
-
Folkerts, J., Stadhouders, R., Redegeld, F. A., Tam, S., Hendriks, R. W., Galli, S. J., & Maurer, M. (2018). Effect of Dietary Fiber and Metabolites on Mast Cell Activation and Mast Cell-Associated Diseases. pmc.ncbi.nlm.nih.gov. https://doi.org/10.3389/fimmu.2018.01067
-
Gutiérrez-Brito, J. A., Lomelí-Nieto, J. Á., Muñoz-Valle, J. F., Oregon-Romero, E., Corona-Angeles, J. A., & Hernández-Bello, J. (2025). Sex hormones and allergies: Exploring the gender differences in immune responses. Frontiers in Allergy, 5, Artículo 1483919. https://doi.org/10.3389/falgy.2024.1483919
-
Rama, T. A., & Silva, D. (2022). Anisakis Allergy: Raising awareness. Acta Médica Portuguesa, 35(7-8), 578-583. https://doi.org/10.20344/amp.15908
-
De las Vecillas, L., Muñoz-Cacho, P., López-Hoyos, M., Monttecchiani, V., Martínez-Sernández, V., Ubeira, F. M., & Rodríguez-Fernández, F. (2020). Analysis of Ani s 7 and Ani s 1 allergens as biomarkers of sensitization and allergy severity in human anisakiasis. Scientific Reports, 10(1). https://doi.org/10.1038/s41598-020-67786-w
-
Cardona, V., Ansotegui, I. J., Ebisawa, M., El-Gamal, Y., Fernandez-Rivas, M., Fineman, S., ... & Worm, M. (2020). World Allergy Organization anaphylaxis guidance 2020. World Allergy Organization Journal, 13(10), 100472. https://doi.org/10.1016/j.waojou.2020.100472
-
Hammad, H., & Lambrecht, B. N. (2021). The basic immunology of asthma. Cell, 184(6), 1469-1485. https://doi.org/10.1016/j.cell.2021.02.016
-
Maspero, J., Adir, Y., Al-Ahmad, M., Celis-Preciado, C. A., Colodenco, F. D., Giavina-Bianchi, P., ... & Yorgancioglu, A. (2022). Type 2 inflammation in asthma and other airway diseases. ERJ Open Research, 8(3). https://doi.org/10.1183/23120541.00576-2021
-
Hill, D. A., & Spergel, J. M. (2018). The atopic march: Critical evidence and clinical relevance. Annals of Allergy, Asthma & Immunology, 120(2), 131–137. https://doi.org/10.1016/j.anai.2017.10.037
-
Pecoraro, L., Mastrorilli, C., Arasi, S., Barni, S., Caimmi, D., Chiera, F., Dinardo, G., Gracci, S., Del Giudice, M. M., Bernardini, R., & Giannetti, A. (2024). Nutritional and Psychosocial Impact of Food Allergy in Pediatric Age. Life, 14(6), 695. https://doi.org/10.3390/life14060695
-
Ryu, S., Lee, K. H., Tizaoui, K., Terrazzino, S., Cargnin, S., Effenberger, M., Shin, J. I., & Kronbichler, A. (2020). Pathogenesis of Eosinophilic Esophagitis: A Comprehensive Review of the Genetic and Molecular Aspects. International Journal Of Molecular Sciences, 21(19), 7253. https://doi.org/10.3390/ijms21197253
-
Santos, A. F., Riggioni, C., Agache, I., Akdis, C. A., Akdis, M., Alvarez‐Perea, A., Alvaro‐Lozano, M., Ballmer‐Weber, B., Barni, S., Beyer, K., Bindslev‐Jensen, C., Brough, H. A., Buyuktiryaki, B., Chu, D., Del Giacco, S., Dunn‐Galvin, A., Eberlein, B., Ebisawa, M., Eigenmann, P., . . . Skypala, I. (2024). EAACI guidelines on the management of IgE‐mediated food allergy. Allergy, 80(1), 14-36. https://doi.org/10.1111/all.16345
-
IgE (Total) Allergy Test - South Tees Hospitals NHS Foundation Trust. (2022, 27 abril). South Tees Hospitals NHS Foundation Trust. https://www.southtees.nhs.uk/services/pathology/tests/ige-total-allergy-test/#:~:text=IgE%20%28Total%29%20Allergy%20Test%20,allergic%20bronchopulmonary%20aspergillosis%2C%20parasitic%20diseases
-
Li, S., Li, J., Zhang, Y., & Zhang, L. (2025). The role of immunoglobulin E in upper respiratory allergies: mechanisms and therapeutic strategies. Immunological Medicine. https://doi.org/10.1080/25785826.2025.2587474
-
Shamji, M. H., Valenta, R., Jardetzky, T., Verhasselt, V., Durham, S. R., Würtzen, P. A., & van Neerven, R. J. J. (2021). The role of allergen-specific IgE, IgG and IgA in allergic disease. Allergy, 76(12), 3627–3641. https://doi.org/10.1111/all.14908
-
Dramburg, S., Hilger, C., Santos, A. F., & de las Vecillas, L. (2023). EAACI Molecular Allergology User's Guide 2.0. Pediatric Allergy and Immunology, 34(S28). https://doi.org/10.1111/pai.13854
-
Kowalski, M. L., Ansotegui, I., Aberer, W., Al-Ahmad, M., Akdis, M., Ballmer-Weber, B. K., Beyer, K., Blanca, M., Brown, S., Bunnag, C., Hulett, A. C., Castells, M., Chng, H. H., De Blay, F., Ebisawa, M., Fineman, S., Golden, D. B., Haahtela, T., Kaliner, M., . . . Zuberbier, T. (2016). Risk and safety requirements for diagnostic and therapeutic procedures in allergology: World Allergy Organization Statement. World Allergy Organization Journal, 9(1), 33. https://doi.org/10.1186/s40413-016-0122-3
-
Garg, V., Brod, B., & Gaspari, A. A. (2021). Patch testing: Uses, systems, risks/benefits, and its role in managing the patient with contact dermatitis. Clinics In Dermatology, 39(4), 580-590. https://doi.org/10.1016/j.clindermatol.2021.03.005
-
Davis, E. C., Castagna, V. P., Sela, D. A., Hillard, M. A., Lindberg, S., Mantis, N. J., Seppo, A. E., & Järvinen, K. M. (2022). Gut microbiome and breast-feeding: Implications for early immune regulation. Journal of Allergy and Clinical Immunology, 150(3), 523–534. https://doi.org/10.1016/j.jaci.2022.07.014
-
Lodge, C., Tan, D., Lau, M., Dai, X., Tham, R., Lowe, A., Bowatte, G., Allen, K., & Dharmage, S. (2015). Breastfeeding and asthma and allergies: a systematic review and meta‐analysis. Acta Paediatrica, 104(S467), 38-53. https://doi.org/10.1111/apa.13132
-
D’Auria, E., Salvatore, S., Acunzo, M., Peroni, D., Pendezza, E., Di Profio, E., Fiore, G., Zuccotti, G. V., & Verduci, E. (2021). Hydrolysed Formulas in the Management of Cow’s Milk Allergy: New Insights, Pitfalls and Tips. Nutrients, 13(8), 2762. https://doi.org/10.3390/nu13082762